导读
动脉粥样硬化(atherosclerosis,AS)是一种缓慢型临床疾病,是心血管疾病的核心,是引起心肌梗死、中风和周围血管疾病的导火索[1]。脂质代谢异常造成的脂质沉积是动脉粥样硬化最直接的致病因素,受累动脉病变从内膜开始,积聚的脂质外观呈黄色粥样,一般先有脂质和复合糖类的异常沉积,进而纤维组织增生及钙质沉着,并伴随着动脉中层逐渐蜕变和钙化,导致动脉壁增厚变硬、失去弹性以及血管腔狭窄。
随着血管逐渐狭窄,病变又会累及不同器官,出现头晕、心痛、胸闷和顽固性高血压、糖尿病等症状,可以说动脉粥样硬化就像一颗“不定时炸弹”。目前我国是全球动脉粥样硬化疾病高发区,60岁以上老年人的发病率高达79.9%;并且近几年偏于年轻化趋势,严重影响人类的生命健康。
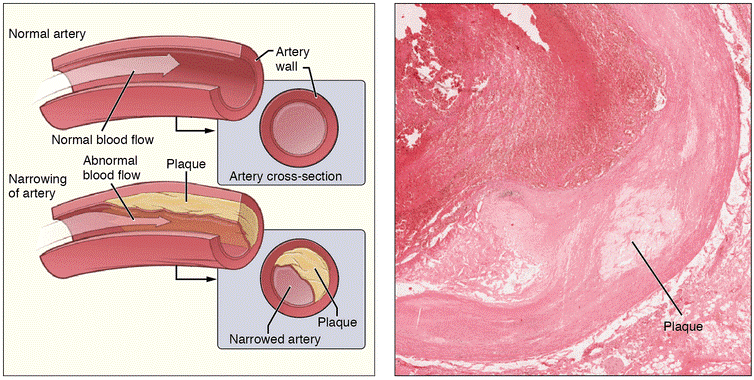
动脉粥样硬化及动脉斑块简图[2]
动脉粥样硬化是多因素共同作用引起的,发病机制较为复杂且尚未完全阐明。目前来看,大小鼠是动脉粥样硬化研究中最常用的物种,尽管有局限性,但其与人类的动脉粥样硬化过程的许多关键特征是相似的,仍然是动脉粥样硬化模型的首选物种。
动脉粥样硬化的发展与胆固醇运输颗粒低密度脂蛋白(LDL)密切相关[3],主要为载脂蛋白E(ApoE)基因和低密度脂蛋白受体(LDLR)基因,可为动脉粥样硬化的治疗和预防提供参考依据。
B-Apoe KO小鼠
载脂蛋白E(Apolipoprotein E, ApoE)是一种与脂质颗粒相关的载体蛋白,主要由肝脏和外周组织中的巨噬细胞产生,是血浆脂蛋白的核心成分。ApoE将脂蛋白、脂溶性维生素和胆固醇输送到淋巴系统,然后进入血液,防止富含胆固醇的颗粒在血浆中积聚,是预防、治疗动脉粥样硬化血管疾病的主要靶点基因。研究表明,ApoE能够通过多种方式预防动脉粥样硬化[4]:促进循环系统中富含甘油三酯的脂蛋白的有效吸收;维持正常的巨噬细胞脂质稳态;调节免疫功能等。
百奥动物BioMice利用基因编辑技术构建了B-Apoe KO小鼠。利用高脂饮食喂养诱导的小鼠胆固醇水平升高程度加大,硬块的形成进一步加剧,类似于人类动脉粥样硬化及动脉粥样硬化性心脏病中的饮食依赖性,可用于心血管疾病及阿尔兹海默症的研究。
B-Apoe KO小鼠特殊饮食诱导动脉粥样硬化模型的建立
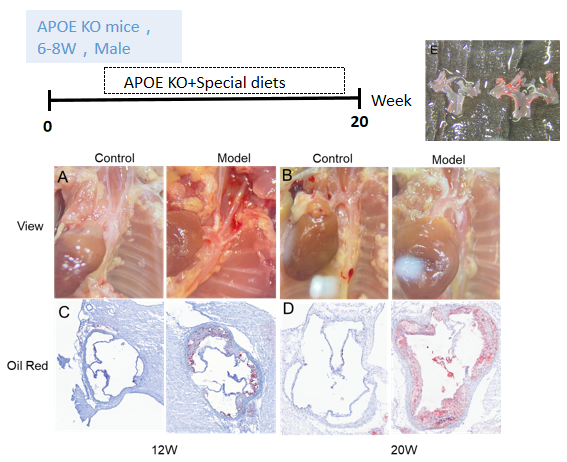
(A-B)小鼠在12周和20周时的动脉粥样硬化斑块。(C-D)主动脉窦在第12周和第20周的油红结果。(E)12周时主动脉弓大体染色。
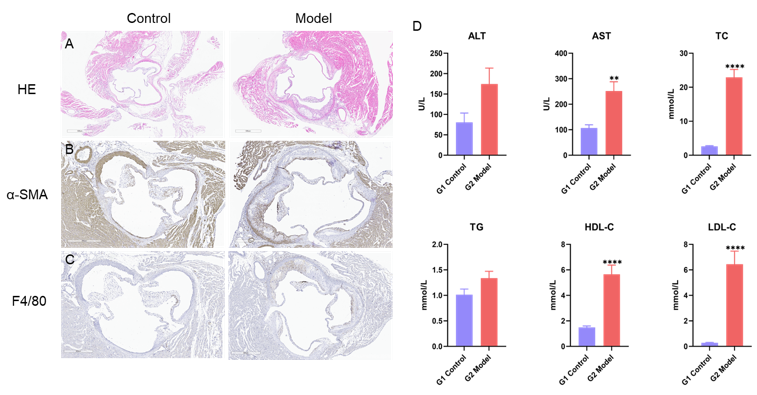
12周时动脉粥样硬化小鼠模型的组织染色和血液生化结果(A)主动脉窦的H&E结果增加。(B-C)免疫组化显示α-SMA和F4/80的表达。(D)血清ALT、AST、TC、TG、HDL-C和LDL-C水平。数值以平均值±SEM表示。**p<0.01,***p<0.001。
B-Ldlr KO大鼠
B-Ldlr KO大鼠的模型验证及分析
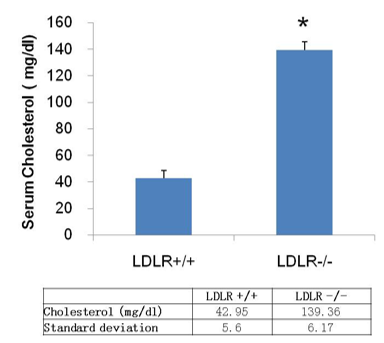
纯合Ldlrtm1/Bcgen大鼠在4个月大时表现出显著升高的血清胆固醇水平。
PCSK与动脉粥样硬化的关系
除了ApoE和LDLR基因外,还有其他与血脂调控相关的类似于PCSK9等靶点用于构建动脉粥样硬化模型,这些模型具有不同的致病机制和病理表型,助力动脉粥样硬化和高脂血症等疾病的研究及治疗药物的开发[6]。
PCSK9是近年来在降脂药开发领域研究的一个新兴靶点,主要在肝脏中表达。PCSK9在LDL-C代谢中发挥重要作用。在肝细胞质膜,分泌的PCSK9的催化结构域与LDL-R结合并被内化,进入内体途径。内体的低pH值增强了PCSK9对LDL-R的亲和力,防止受体再循环到细胞表面。而PCSK9与LDL-R结合后再与LDL-C结合形成新的复合体进入溶酶体中一起被降解,最终导致LDL-R 减少,LDL-C的降解随之减少,从而使LDL-C的水平升高[7]。
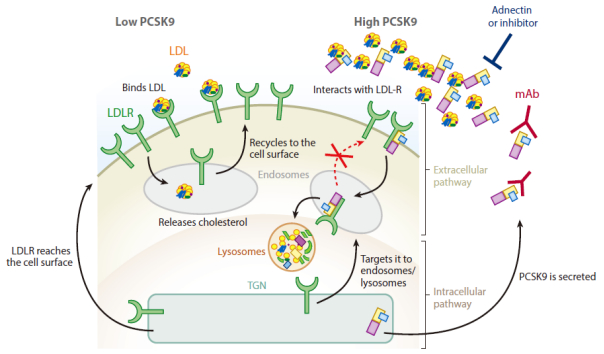
PCSK9 在 LDL 受体 (LDL-R) 代谢中的作用[7]
脂质代谢分析
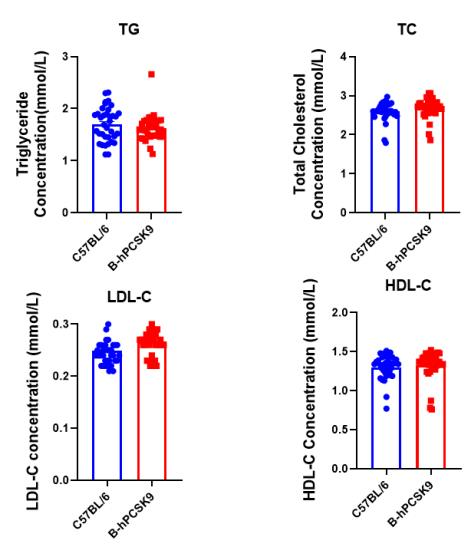
B-hPCSK9 小鼠的脂质代谢分析。分析 B-hPCSK9 小鼠和野生型 C57BL/6 小鼠(n=36,6周)TG、TC、LDL-C和 HDL-C 的血浆浓度。B-hPCSK9小鼠和野生型 C57BL/6 小鼠之间无差异。TG:甘油三酯;TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇。
药效验证
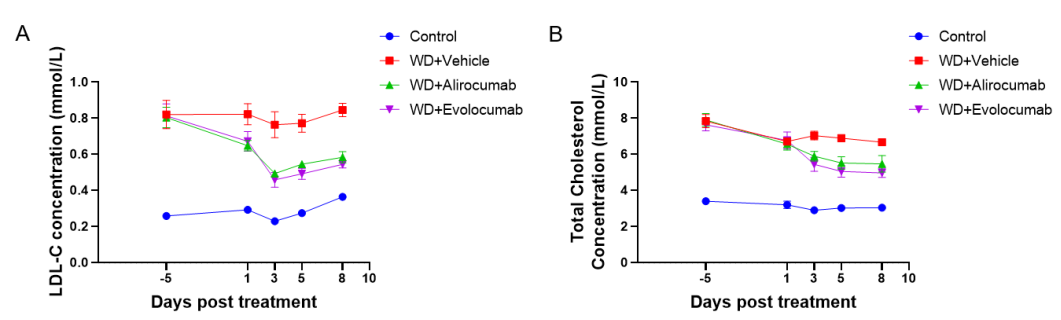
抗人 PCSK9 抗体在 WD 诱导 B-hPCSK9 小鼠的体内有效性。B-hPCSK9 小鼠给予Alirocumab(内部)/Evolocumab(内部)或同型对照抗体(单次给药,s.c.)(n=8,雄鼠)。在第-5、1、3、5和8天采集血液进行分析。与同型对照相比,抗人 PCSK9 抗体给药组小鼠的血清 LDL-C(A) 和 TC(B) 水平降低,表明抗人 PCSK9 抗体可有效控制雄性 B-hPCSK9 小鼠的血脂。数值表示为平均值±SEM。TC:总胆固醇;LDL-C:低密度脂蛋白胆固醇。WD:西方饮食。
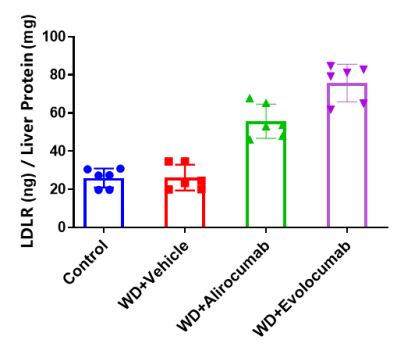
抗人 PCSK9 抗体上调 B-hPCSK9 小鼠的 LDLR 水平。B-hPCSK9 小鼠给予Alirocumab(内部)/Evolocumab(内部)或同型对照抗体(单次给药,s.c.)(n=6,雄鼠)。在第8天采集肝组织用于 ELISA 分析。与同种型对照相比,抗人 PCSK9 抗体给药组小鼠中 LDLR 水平上调。数值表示为平均值±SEM。LDLR:低密度脂蛋白胆固醇受体。WD:西方饮食。
表1. 动脉粥样硬化相关小鼠模型

参考文献
[1]Besa Emini Veseli,Paola PerrottaEuropean Journal of Pharmacology,Animal models of atherosclerosis,Volume 816, 5 December 2017.
[2]Wikipedia/CC BY 3.0
[3]Godfrey, S, Getz, Catherine, A, & Reardon. (2012). Animal models of atherosclerosis. Arteriosclerosis Thrombosis & Vascular Biology.
[4]Jean Davignon, Jeffrey S.Cohn, et al. Apolipoprotein E and atherosclerosis: insight from animal and human studies.Clinica Chimica Acta.Clinica Chimica Acta.
[5]Brown, Michael S, and Joseph L. Goldstein. A receptor-mediated pathway for cholesterol homeostasis. Science232.4746(1986): 34-47.
[6]Gresham, G. A. (2017). Animal models of atherosclerosis. Biomedical Reports, 6(3), 259-266.
[7]Hess, C. N., Low Wang, C. C. & Hiatt, W. R. PCSK9 Inhibitors: Mechanisms of Action, Metabolic Effects, and Clinical Outcomes. Annual review of medicine 69, 133-145