百奥赛图是一家创新技术驱动新药研发的国际性生物技术公司,致力于成为全球新药发源地,以专注技术创新、持续新药产出、守护人类健康为使命。基于百奥赛图自主研发并拥有完全独立知识产权的全人抗体RenMab®、RenLite®、RenNano®小鼠,将单细胞抗体发现技术平台、高效的基因编辑模型开发平台、规模化动物模型供应平台、快速的动物体内外药效评价平台、强大的临床开发能力有机整合在一起,形成了独具特色、涵盖药物研发全流程的新药研发体系。公司成功战略升级为Biotech,未来将更聚焦于创新抗体药物研发。随着规模化抗体药物研发-“千鼠万抗TM”计划的实施,百奥赛图将携手全球合作伙伴,共同加速新药研发。百奥赛图总部位于北京,在江苏海门、美国波士顿、上海等地设有分支机构,全资子公司祐和医药专注于临床开发。
[更多详情]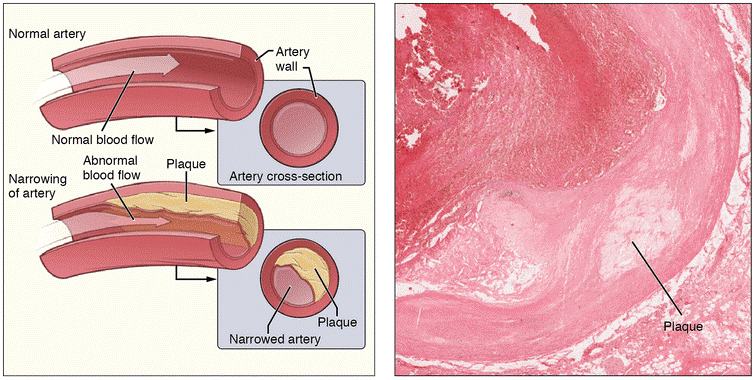
导读
动脉粥样硬化(atherosclerosis,AS)是一种缓慢型临床疾病,是心血管疾病的核心,是引起心肌梗死、中风和周围血管疾病的导火索[1]。脂质代谢异常造成的脂质沉积是动脉粥样硬化最直接的致病因素,受累动脉病变从内膜开始,积聚的脂质外观呈黄色粥样,一般先有脂质和复合糖类的异常沉积,进而纤维组织增生及钙质沉着,并伴随着动脉中层逐渐蜕变和钙化,导致动脉壁增厚变硬、失去弹性以及血管腔狭窄。
随着血管逐渐狭窄,病变又会累及不同器官,出现头晕、心痛、胸闷和顽固性高血压、糖尿病等症状,可以说动脉粥样硬化就像一颗“不定时炸弹”。目前我国是全球动脉粥样硬化疾病高发区,60岁以上老年人的发病率高达79.9%;并且近几年偏于年轻化趋势,严重影响人类的生命健康。
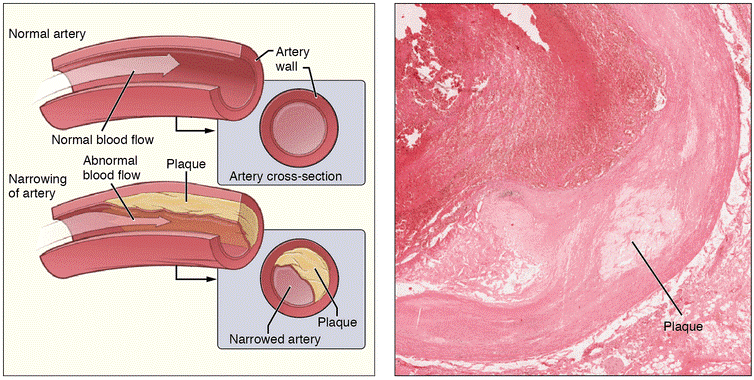
动脉粥样硬化及动脉斑块简图[2]
动脉粥样硬化是多因素共同作用引起的,发病机制较为复杂且尚未完全阐明。目前来看,大小鼠是动脉粥样硬化研究中最常用的物种,尽管有局限性,但其与人类的动脉粥样硬化过程的许多关键特征是相似的,仍然是动脉粥样硬化模型的首选物种。
动脉粥样硬化的发展与胆固醇运输颗粒低密度脂蛋白(LDL)密切相关[3],主要为载脂蛋白E(ApoE)基因和低密度脂蛋白受体(LDLR)基因,可为动脉粥样硬化的治疗和预防提供参考依据。
B-Apoe KO小鼠
载脂蛋白E(Apolipoprotein E, ApoE)是一种与脂质颗粒相关的载体蛋白,主要由肝脏和外周组织中的巨噬细胞产生,是血浆脂蛋白的核心成分。ApoE将脂蛋白、脂溶性维生素和胆固醇输送到淋巴系统,然后进入血液,防止富含胆固醇的颗粒在血浆中积聚,是预防、治疗动脉粥样硬化血管疾病的主要靶点基因。研究表明,ApoE能够通过多种方式预防动脉粥样硬化[4]:促进循环系统中富含甘油三酯的脂蛋白的有效吸收;维持正常的巨噬细胞脂质稳态;调节免疫功能等。
百奥动物BioMice利用基因编辑技术构建了B-Apoe KO小鼠。利用高脂饮食喂养诱导的小鼠胆固醇水平升高程度加大,硬块的形成进一步加剧,类似于人类动脉粥样硬化及动脉粥样硬化性心脏病中的饮食依赖性,可用于心血管疾病及阿尔兹海默症的研究。
B-Apoe KO小鼠特殊饮食诱导动脉粥样硬化模型的建立
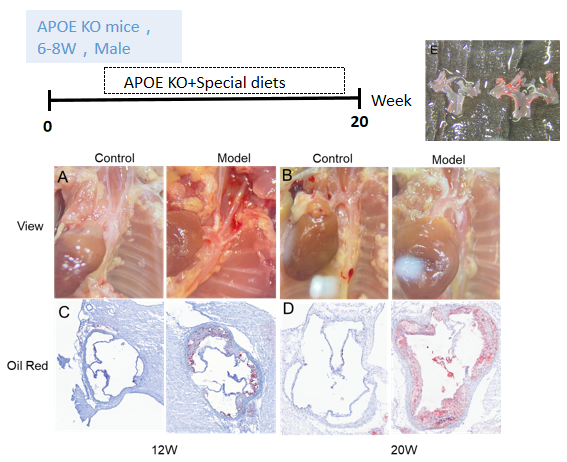
(A-B)小鼠在12周和20周时的动脉粥样硬化斑块。(C-D)主动脉窦在第12周和第20周的油红结果。(E)12周时主动脉弓大体染色。
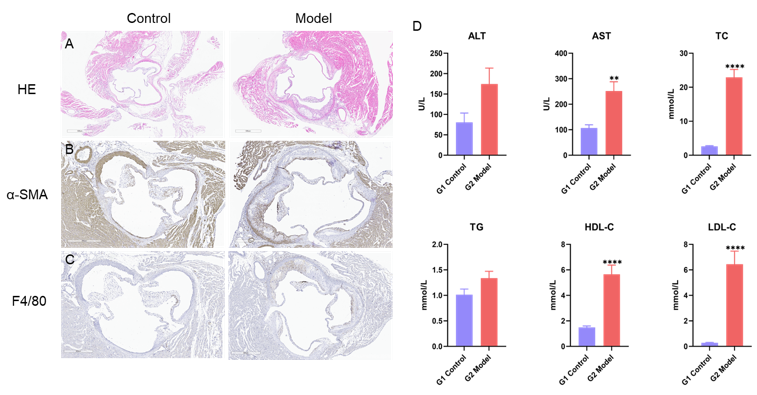
12周时动脉粥样硬化小鼠模型的组织染色和血液生化结果(A)主动脉窦的H&E结果增加。(B-C)免疫组化显示α-SMA和F4/80的表达。(D)血清ALT、AST、TC、TG、HDL-C和LDL-C水平。数值以平均值±SEM表示。**p<0.01,***p<0.001。
B-Ldlr KO大鼠
B-Ldlr KO大鼠的模型验证及分析
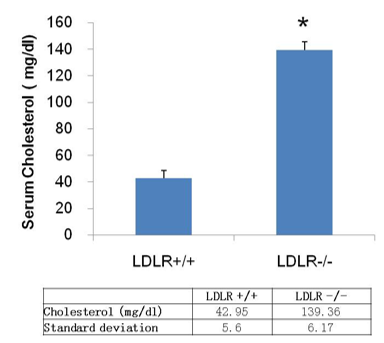
纯合Ldlrtm1/Bcgen大鼠在4个月大时表现出显著升高的血清胆固醇水平。
PCSK与动脉粥样硬化的关系
除了ApoE和LDLR基因外,还有其他与血脂调控相关的类似于PCSK9等靶点用于构建动脉粥样硬化模型,这些模型具有不同的致病机制和病理表型,助力动脉粥样硬化和高脂血症等疾病的研究及治疗药物的开发[6]。
PCSK9是近年来在降脂药开发领域研究的一个新兴靶点,主要在肝脏中表达。PCSK9在LDL-C代谢中发挥重要作用。在肝细胞质膜,分泌的PCSK9的催化结构域与LDL-R结合并被内化,进入内体途径。内体的低pH值增强了PCSK9对LDL-R的亲和力,防止受体再循环到细胞表面。而PCSK9与LDL-R结合后再与LDL-C结合形成新的复合体进入溶酶体中一起被降解,最终导致LDL-R 减少,LDL-C的降解随之减少,从而使LDL-C的水平升高[7]。
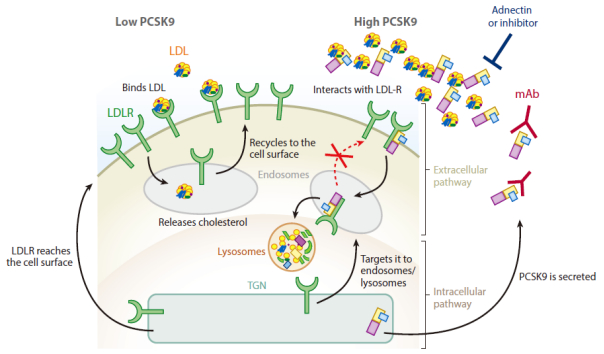
PCSK9 在 LDL 受体 (LDL-R) 代谢中的作用[7]
脂质代谢分析
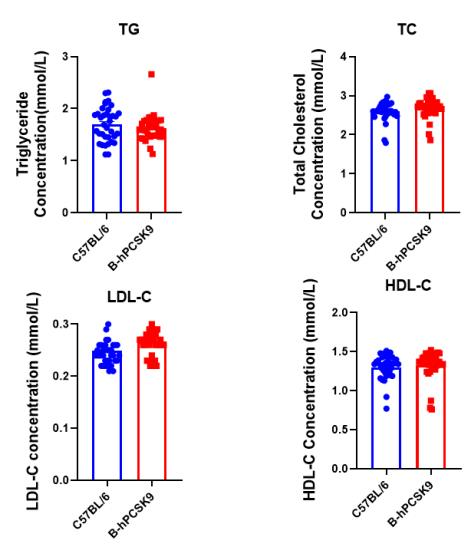
B-hPCSK9 小鼠的脂质代谢分析。分析 B-hPCSK9 小鼠和野生型 C57BL/6 小鼠(n=36,6周)TG、TC、LDL-C和 HDL-C 的血浆浓度。B-hPCSK9小鼠和野生型 C57BL/6 小鼠之间无差异。TG:甘油三酯;TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇。
药效验证
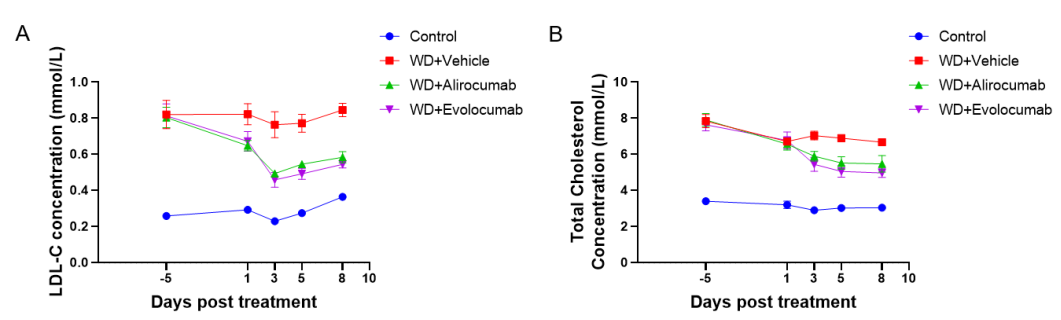
抗人 PCSK9 抗体在 WD 诱导 B-hPCSK9 小鼠的体内有效性。B-hPCSK9 小鼠给予Alirocumab(内部)/Evolocumab(内部)或同型对照抗体(单次给药,s.c.)(n=8,雄鼠)。在第-5、1、3、5和8天采集血液进行分析。与同型对照相比,抗人 PCSK9 抗体给药组小鼠的血清 LDL-C(A) 和 TC(B) 水平降低,表明抗人 PCSK9 抗体可有效控制雄性 B-hPCSK9 小鼠的血脂。数值表示为平均值±SEM。TC:总胆固醇;LDL-C:低密度脂蛋白胆固醇。WD:西方饮食。
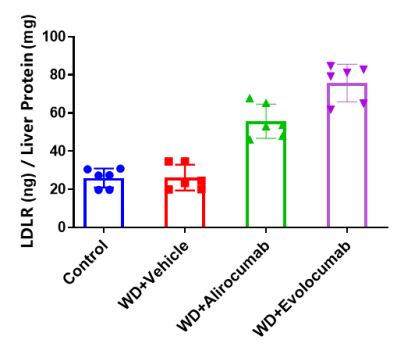
抗人 PCSK9 抗体上调 B-hPCSK9 小鼠的 LDLR 水平。B-hPCSK9 小鼠给予Alirocumab(内部)/Evolocumab(内部)或同型对照抗体(单次给药,s.c.)(n=6,雄鼠)。在第8天采集肝组织用于 ELISA 分析。与同种型对照相比,抗人 PCSK9 抗体给药组小鼠中 LDLR 水平上调。数值表示为平均值±SEM。LDLR:低密度脂蛋白胆固醇受体。WD:西方饮食。
表1. 动脉粥样硬化相关小鼠模型

参考文献
[1]Besa Emini Veseli,Paola PerrottaEuropean Journal of Pharmacology,Animal models of atherosclerosis,Volume 816, 5 December 2017.
[2]Wikipedia/CC BY 3.0
[3]Godfrey, S, Getz, Catherine, A, & Reardon. (2012). Animal models of atherosclerosis. Arteriosclerosis Thrombosis & Vascular Biology.
[4]Jean Davignon, Jeffrey S.Cohn, et al. Apolipoprotein E and atherosclerosis: insight from animal and human studies.Clinica Chimica Acta.Clinica Chimica Acta.
[5]Brown, Michael S, and Joseph L. Goldstein. A receptor-mediated pathway for cholesterol homeostasis. Science232.4746(1986): 34-47.
[6]Gresham, G. A. (2017). Animal models of atherosclerosis. Biomedical Reports, 6(3), 259-266.
[7]Hess, C. N., Low Wang, C. C. & Hiatt, W. R. PCSK9 Inhibitors: Mechanisms of Action, Metabolic Effects, and Clinical Outcomes. Annual review of medicine 69, 133-145
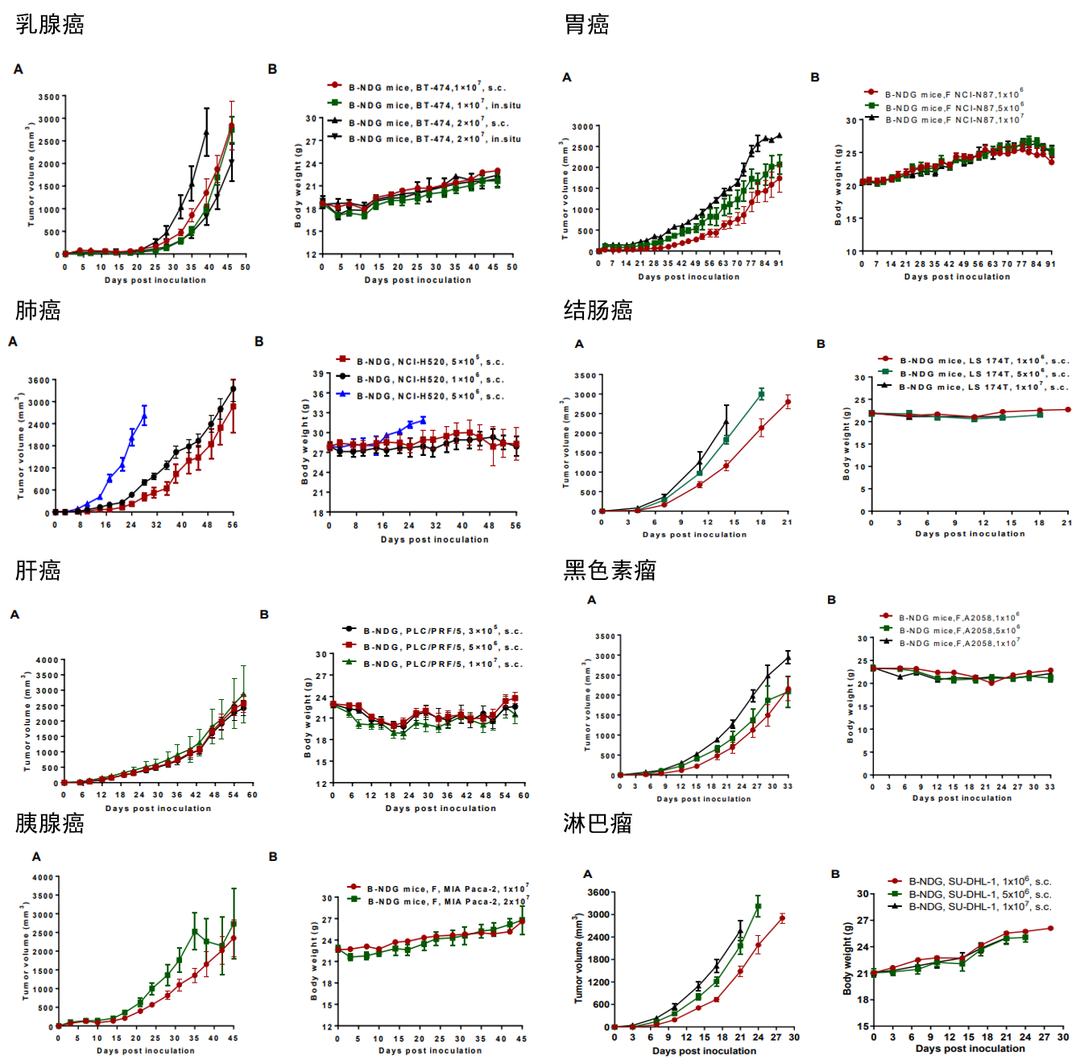
肿瘤动物模型的建立为研究肿瘤发生与转移的机制、筛选和评价抗肿瘤药物的药效提供了有力的工具。啮齿类动物小鼠,因为其具有繁育速度快,成本低,可进行基因修饰等诸多优点,基于其构建的各类肿瘤模型构成了临床前治疗性药物筛选的主要工具。小鼠肿瘤模型大致可分为自发性肿瘤小鼠模型、诱发性肿瘤小鼠模型、基因工程小鼠肿瘤模型、异种移植瘤模型(PDX或CDX)等。 重建了人免疫系统的异种移植小鼠肿瘤模型(CDX或PDX)可同时具备人免疫系统和人肿瘤组织,更接近人体真实情况,实现了在动物体内模拟人类免疫系统和肿瘤之间的相互作用。 细胞系异种移植模型(Cell line-derived xenograft, CDX)是将体外培养的人源的肿瘤细胞系通过皮下、静脉或者原位的方式接种至重度免疫缺陷小鼠(如B-NDG小鼠)或者是人源化免疫系统小鼠体内而构建的肿瘤模型。基于细胞系的肿瘤模型作为经典的体内实验方法,在肿瘤学研究和抗肿瘤药物研发过程中有着极大的需求。 CDX模型具有实验周期短、建模成功率高、重复性高、动物个体成瘤差异较小、实验费用相对低等优点,可以用于开展药物靶点验证、药效学评价、PK/PD研究和多药协同药效评价等,是评估抗肿瘤药物免疫治疗效果的重要临床前动物模型。 图1. 异种移植小鼠肿瘤模型 小鼠的CDX成瘤模型 CDX皮下模型 以重度免疫缺陷小鼠为例,我们已经完成了25种肿瘤细胞系的CDX模型构建,包括结肠癌、肺癌、乳腺癌、肝癌、胃癌、胰腺癌、淋巴瘤和黑色素瘤等。 以下是百奥动物基于B-NDG小鼠建立的部分CDX成瘤模型展示。 图2. B-NDG小鼠CDX模型成瘤数据 CDX原位模型 关于原位移植肿瘤模型,想要了解更多,请点击上图。 CDX淋巴癌转移模型 图3. Raji淋巴肿瘤细胞在B-NDG小鼠上能更有效地建立系统和转移肿瘤模型 对B-NDG、NOD-scid BALB/C Nude小鼠通过尾静脉注射相同数量 (5× 105)的Raji细胞,在不同的时间点记录并分析小鼠的如下各种指标: (A) 细胞接种后记录小鼠生存情况,绘制Kaplan-Merier生存曲线。 (B)细胞接种后每周小鼠体重变化(g),并计算出相对于接种当天的相对体重 (C)小鼠外周血中人源细胞百分率变化。接种Raji細胞后,每周通过眼眶静脉丛采取100 以μl全血,提取DNA,通过q-PCR技术检测小鼠外周血中人源细胞比率。 (D)接种Raji细胞后小鼠肝脏对比。接种后待小鼠体重下降超过30%后执行安乐死并解剖脏器,进行拍照。 (E)接种Raji细胞后小鼠脏器免疫组化染色。一抗为鼠抗人线粒体膜蛋白抗体。 结果表明,相对于NOD-scid小鼠B-NDG小鼠更适合建立人源肿瘤模型。 利用CDX肿瘤模型进行药物体内药效评价 B-NDG小鼠CDX淋巴瘤体内药效实验 图4. 基于B-NDG小鼠的Raji淋巴癌转移模型及药效评价 对B-NDG小鼠通过尾静脉注射相同数量(5x105)的Raji-Fluc细胞,并在第3天以及第10天尾静脉注射相同剂量的抗体X,之后在不同的时间点成像观察肿瘤生长状况。(A)不同时间点对小鼠成像观察肿瘤生长情况;(B)不同分组小鼠成像下肿瘤细胞荧光强度曲线。结果表明,早起抗体治疗(Raji细胞移植3天,10天给药)的治疗效果显著,晚期抗体治疗(Raji细胞移植10天给药)的治疗效果明显变差,基本无效。 B-NDG小鼠CDX模型抗人CD47抗体药效验证实验 图5. B-NDG小鼠抗人CD47抗体的抗肿瘤活性 将人淋巴B-lciferase-GFP Raji细胞(B ymphocytes)细胞通过尾静脉注射到B-NDG小鼠体内,利用小动物成像仪进行观察,待肿瘤荧光强度达到1E+06左右时将动物入组至对照组和治疗组(n=6)。(A)荧光成像仪监测小鼠肿瘤荧光,(B)治疗期间的体重变化。结果表明,3种抗体对B-NDG小鼠的肿瘤生长抑制均有效果。B-NDG小鼠是人CD47抗体有效性研究的有力模型。数值表示为平均值±SEM。 B-NDG小鼠CDX模型CAR-T药效验证实验 图6. CAR-T疗法在B-NDG小鼠中的抗肿瘤活性 将B-luciferase-GFP Raji细胞(B lymphocytes)通过尾静脉植入B-NDG小鼠。当荧光强度达到约1E+06(n=6)时,将小鼠分组,用CAR-T细胞(1E+07)处理。(A)Raji-Luciferase细胞系经不同CAR-T细胞处理后的信号强度,(B)处理期间的体重变化。结果显示,4种CAR-T细胞在B-NDG小鼠中表现出不同地抑制肿瘤生长活性。结果表明,B-NDG小鼠可以作为CAR-T细胞治疗研究的有力模型。数值表示为平均值±SEM。 B-NDG小鼠CDX模型ADC药效验证实验 图7. ADC药物在几种CDX模型中的体内抗肿瘤疗效研究 采用不同抗原表达水平的细胞系验证ADC药物的体内药效水平。如图7所示,在皮下接种了BT474和NCI-H1975的B-NDG小鼠肿瘤模型中,所有受试品ADC对肿瘤生长均表现出明显的抑制作用。在A431肿瘤模型中的抑制作用相对较弱,这与A431细胞上HER2的低表达水平相一致。 CDX模型列表 BioMice百奥动物一直在追求创新、不断的探索,以期为广大科研工作者提供优质的小鼠模型,助力科学研究以及药物开发! 如您有关注的肿瘤相关动物模型,欢迎联系我们,获取更多百奥动物产品信息。








CD47作为第一个被发现的肿瘤吞噬相关检查点,在多种人类血液肿瘤中存在高表达。目前,CD47的一个主要难点是其在红细胞和血小板有表达,导致血液毒性。然而,研究表明,CD24不在人红细胞表达,不会产生贫血的副作用[2]。
作用机制
CD24可作为“别吃我”信号分子,与巨噬细胞上的分子Siglec-10相互作用,传递抑制性信号,抑制破坏性炎症反应,减少巨噬细胞吞噬作用,传递“别吃我”信号。CD24可以与现有疗法互补,是未来免疫治疗的潜在靶点。

CD24-Siglec-10抑制吞噬作用的示意图[3]
研究进展
通过查询统计,目前针对CD24靶点进行开发的在研公司或机构有很多,适应症涉及自身免疫疾病、炎症、病毒感染和肿瘤等多个领域。

随着针对CD24靶点作用机制的发现,需要更多的临床研究来检验靶点对不同类型的肿瘤的影响。百奥动物自研产品B-hCD24 mice plus,是靶向CD24抗体开发相关药物进行药效评价的优质模型。相信随着对CD24的开发,多个领域的药物研发势必会进入一个加速的时代。
数据展示
01
基本信息

02
血红细胞蛋白表达分析

流式细胞术分析纯合B-hCD24小鼠中的种属特异性CD24的表达。采集野生型小鼠和纯合B-hCD24小鼠的红细胞,结合种特异性抗CD24抗体通过流式细胞术进行分析。在野生型小鼠中可检测到小鼠CD24,但在B-hCD24小鼠中未检测到。在纯合B-hCD24小鼠中未检测到人CD24。
03
B细胞蛋白表达分析

流式细胞术分析纯合B-hCD24小鼠中的种属特异性CD24的表达。采集野生型小鼠和纯合B-hCD24小鼠的血细胞和脾细胞,结合种特异性抗CD24抗体通过流式细胞术进行分析。在野生型小鼠血液(A)和脾脏(B)中均可检测到小鼠CD24。在纯合B-hCD24小鼠血液(A)和脾脏(B)中可检测到人CD24。
04
T细胞蛋白表达分析

流式细胞术分析纯合B-hCD24小鼠中的种属特异性CD24的表达。采集野生型小鼠和纯合B-hCD24小鼠的血细胞和脾细胞,结合种特异性抗CD24抗体通过流式细胞术进行分析。在野生型小鼠血液中仅可检测到少量小鼠CD24(A),而在野生型小鼠脾脏中无法检测到小鼠CD24(B)。在纯合B-hCD24小鼠血液(A)和脾脏(B)中均未检测到人CD24。
05
NK细胞蛋白表达分析

流式细胞术分析纯合B-hCD24小鼠中的种属特异性CD24的表达。采集野生型小鼠和纯合B-hCD24小鼠的血细胞和脾细胞,结合种特异性抗CD24抗体通过流式细胞术进行分析。在野生型小鼠血液(A)和脾脏(B)中未检测到小鼠CD24。在纯合B-hCD24小鼠血液(A)和脾脏(B) 中未检测到人CD24。
06
粒细胞蛋白表达分析

流式细胞术分析纯合子B-hCD24小鼠中的种属特异性CD24的表达。采集野生型小鼠和纯合B-hCD24小鼠的血细胞和脾细胞,结合种特异性抗CD24抗体通过流式细胞术进行分析。在野生型小鼠血液(A)和脾脏(B)中可检测到小鼠CD24。在纯合B-hCD24小鼠血液(A)和脾脏 (B)中可检测到人CD24。
07
巨噬细胞蛋白表达分析

流式细胞术分析纯合B-hCD24小鼠中的种属特异性CD24的表达。采集野生型小鼠和纯合B-hCD24小鼠的血细胞和脾细胞,结合种特异性抗CD24抗体通过流式细胞术进行分析。在野生型小鼠血液(A)和脾脏(B)中可检测到小鼠CD24。在纯合B-hCD24小鼠血液(A)和脾脏(B)中可检测到人CD24。
08
树突状细胞蛋白表达分析

流式细胞术分析纯合B-hCD24小鼠中的种属特异性CD24的表达。采集野生型小鼠和纯合B-hCD24小鼠的血细胞和脾细胞,结合种特异性抗CD24抗体通过流式细胞术进行分析。在野生型小鼠血液(A)和脾脏(B)中可检测到小鼠CD24。在纯合B-hCD24小鼠血液(A)和脾脏(B)中可检测到人CD24。
09
CD24表达总结

野生型小鼠与人的CD24表达谱不同,主要差别在于人红细胞不表达CD24但小鼠的红细胞表达。或可导致药物在野生型小鼠体内筛选时,可能会遇到在人中不会出现的血液毒性,干扰药物安全性、有效性的临床前评估。B-hCD24 mice plus人源化小鼠CD24表达谱与人一致,可有效避免相应风险。
髓系细胞检查点相关产品列表

参考资料
1.Song Y, et al. Targeting macrophages in hematological malignancies: recent advances and future directions. J Hematol Oncol. 2022 Aug 17;15(1):110. doi: 10.1186/s13045-022-01328-x.
2.British Journal of Cancer (2013) 108, 1449–1459 | doi: 10.1038/bjc.2013.102
3.Amira A Barkal, Irving L Weissman. CD24 signalling through macrophage Siglec-10 is a target for cancer immunotherapy. Nature. 2019 Aug;572(7769):392-396.
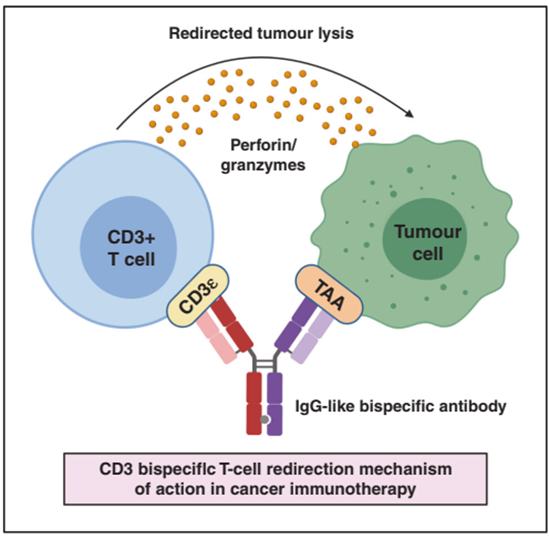
CD3 双抗介绍 CD3×TAA双抗的作用机制[1] CD3双抗最新研究进展 数据来源于科睿唯安及公开信息整理 BioMice百奥动物自主研发了多个CD3×TAA小鼠模型,为双抗或三抗或多抗药物体内药效和安全性评价提供了有力工具。部分数据展示如下。 B-hCD3E mice 基本信息 功能分析:体外刺激T细胞分泌细胞因子及双抗体外杀伤 人源化小鼠的T细胞,在体外经CD3+ CD28刺激后,IL-2分泌增加,表明人源化改造后Th1细胞功能正常。人源化小鼠脾细胞+过表达MC38 细胞系+双抗孵育48h后,检测细胞裂解产生的LDH,结果显示CD8+ T细胞功能正常。 双抗药效验证 B-hCD3E mice+MC38-hCD19 接种MC38-hEpCAM至B-hCD3E纯合小鼠皮下,肿瘤组织接近150±50mm3时分组进行体内药效评价实验(n=6)。 结果显示高剂量hCD3E抗体(Blinatumomab)可显著抑制肿瘤生长,证明B-hCD3E小鼠模型是体内评价抗hCD3E双特异性抗体疗效的有力工具。 单抗药效验证 人源化小鼠中mPD-1抗体显著抑制肿瘤生长(A),这表明CD3E人源化没有影响T细胞功能。抗hCD3抗体处理后肿瘤生长较快(A),B细胞占比没有明显差异(B),T细胞占比明显下降(C),这表明hCD3抗体处理的肿瘤快速生长是由于T细胞过度激活耗竭(AICD)导致的。 肿瘤标记物Ab(X)药效验证 人源化小鼠中高剂量CD3双抗X抑制了肿瘤生长(A),治疗期间小鼠体重没有变化(B),B-hCD3E小鼠血液中B细胞(C)和T细胞(D)的比例没有明显变化。CD3双抗X在保持抑瘤效果的同时,没有产生过度激活T细胞的毒性,表明,B-hCD3E小鼠可作为CD3双抗临床前药效和毒性评价有力的研究模型。 三特异性抗体介绍 三特异性抗体拥有三种特异性抗原结合位点,可以同时与靶细胞、功能细胞(一般为T细胞)相互作用,进而增强对靶细胞的杀伤。与单克隆抗体相比,三抗增加了两个特异性抗原结合位点,有利于将药物重定向至肿瘤局部,增加结合特异性,提升药物靶向肿瘤细胞的准确性,降低脱靶毒性。 三特异性抗体作用机制[2] 三特异性抗体最新研究进展 全球已有多家生物医药企业布局三特异性抗体,赛诺菲作为三抗研发赛道的“领跑者”,目前已有3个三特异性抗体产品进入临床试验I期阶段,其中SAR442257是一款靶向CD3×CD28×CD38的三特异性抗体,它在体外试验中表现出比CD38单克隆抗体高1000~10000倍的骨髓瘤细胞杀伤活性。拟开发的适应症包括多发性骨髓瘤和非霍奇金淋巴瘤。除赛诺菲外还有诺华、罗氏是这一赛道的先行者。国内基石药业、嘉和生物等也都在布局三抗管线。 数据来源于科睿唯安及公开信息整理 B-hCD3E/hCD28 mice 基本信息 蛋白表达分析 取野生型小鼠和纯合B-hCD3E/hCD28小鼠脾细胞,用种属特异性抗CD3E抗体进行流式细胞术分析。如图所示,小鼠CD3E在野生型小鼠中检测到。人CD3E仅在纯合B-hCD3E/hCD28小鼠中检测到,而在野生型小鼠中检测不到(A)。小鼠CD28在野生型小鼠中检测到。人CD28仅在纯合B-hCD3E/hCD28小鼠中检测到,而在野生型小鼠中检测不到(B)。 B-hCD3E/h4-1BB mice 基本信息 蛋白表达分析 取野生型小鼠和纯合B-hCD3E/h4-1BB小鼠脾细胞,用种属特异性抗CD3E抗体进行流式细胞术分析。小鼠CD3E在野生型小鼠中检测到。人CD3E仅在纯合B-hCD3E/h4-1BB小鼠中检测到,而在野生型小鼠中检测不到(A)。用种属特异性抗4-1BB抗体进行流式细胞术分析。小鼠4-1BB在野生型小鼠中检测到。人4-1BB仅在纯合B-hCD3E/h4-1BB小鼠中检测到,而在野生型小鼠中检测不到(B)。 参考文献















1. Singh A, Dees S, Grewal IS. Overcoming the challenges associated with CD3+ T-cell redirection in cancer. Br J Cancer. 2021 Mar;124(6):1037-1048. doi: 10.1038/s41416-020-01225-5. Epub 2021 Jan 19. PMID: 33469153; PMCID: PMC7960983;
2. R&D Investor Event,Adapted from Garfall et al, Trispecific antibodies offer a third way forward for anticancer immunotherapy, Nature 575, 2019 ©2019, Springer Nature (under permission requested). Article screenshot from Wu et al, Trispecific antibodies enhance the therapeutic efficacy of tumor-directed T cells through T cell receptor co-stimulation, Nat Cancer 2020 ©2020, Springer Nature (under permission requested).

随着生活水平的提高以及医疗技术的不断发展,人类预期寿命在逐步延长,这导致全球老年人口的空前增长,与此同时,与年龄相关的疾病负担也呈指数级增长[1]。 有研究指出,在健康状况没有得到改善的情况下单纯延长寿命,是没有意义的[2]。基于此,世界卫生组织在2015年提出了《老龄化与健康全球战略和行动计划》,旨在实现健康老龄化的目标[3]。 为了实现这一目标,需要对生物体、器官和细胞水平的衰老及疾病过程有透彻的了解,并针对衰老相关的分子途径开发预防和治疗衰老相关疾病的策略[4]。
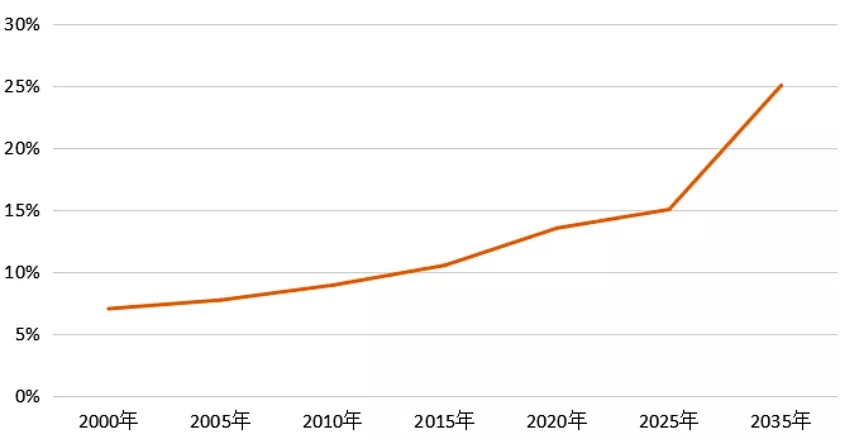
我国65岁以上人口占总人口比重及预测[5]
小鼠凭借其易于饲养和处理并且寿命较短(~2.5年)的特性,成为衰老及其相关疾病研究中有吸引力的哺乳动物模式生物。[7]

老龄鼠
百奥动物老龄鼠优势
① 不同周龄小鼠现货提供;
② 高标准的饲养环境;
③ 非生产退役种鼠;
④ 严格的遗传稳定性监测。
C57BL/6J老龄鼠
C57BL/6J是使用最为广泛的近交品系之一,也是第一个完成基因组测序,特征分析最全面的小鼠品系。有研究人员对C57BL/6J的生存曲线进行分析,并提供了可比较的对应的人类年龄。衰老是个连续的动态过程,大多数研究将生命阶段简单的分为成年、中年和老年。
小鼠月龄和人类年龄对照关系及特点
① 小鼠的3-6月龄对应成年人(20-30岁);
发育完成尚未受到衰老影响。
② 小鼠的10-15月龄对应中年人(38-47岁);
可以检测到部分衰老生物标志物(非全部)的衰老变化。
③ 小鼠的18-24月龄对应老年人(56-69岁);
可以检测到几乎全部衰老标志物的衰老变化[8]。
老龄鼠常见表型及病理
随着小鼠生长发育,外观会逐渐改变。一些常见的衰老表型有:眼周脱毛、嘴鼻部被理毛、背侧产生脱毛区及灰毛区等。

C57BL/6J老龄鼠的部分正常衰老表型[9]
同时随着年龄增长,与年龄相关的各项疾病也随之而来,产生一些和疾病相关的表型。例如:自发肿瘤、眼周病变、皮炎脱毛等。
非近亲繁殖小鼠长期研究(2年或更长时间)的常见疾病[10]
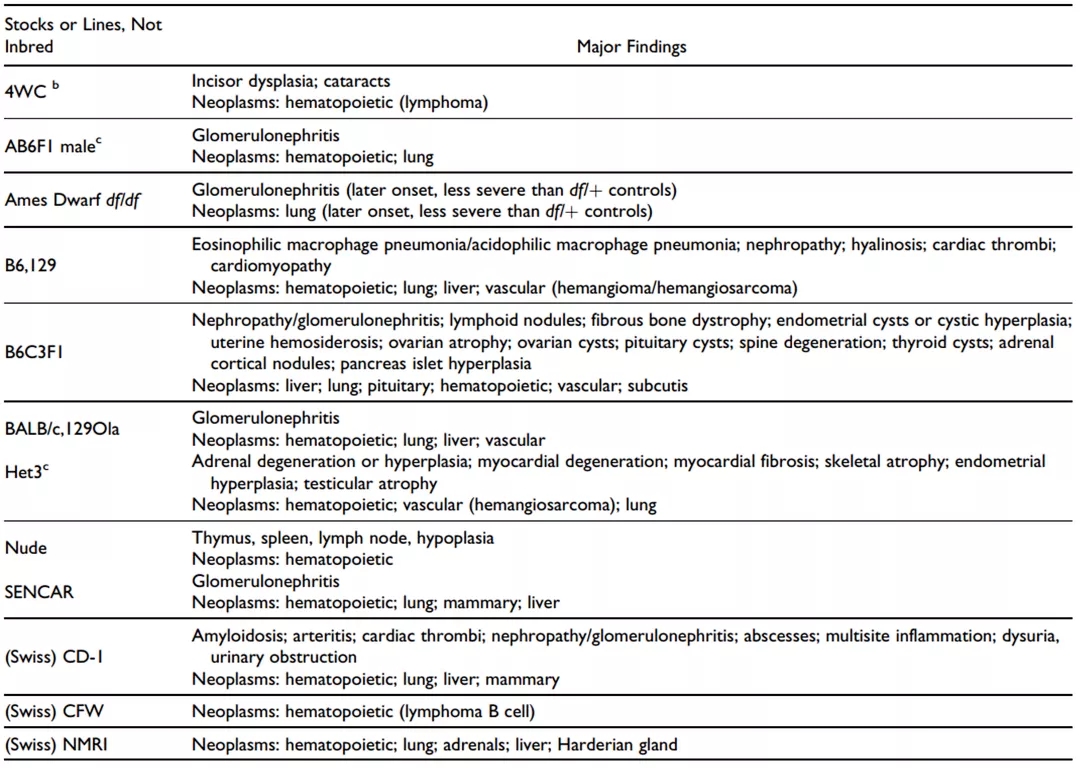
a、Findings from multiple studies are summarized for each line or group. and original terminology.
b、4-way cross
c、(Af _ C57BL/6)F1
d、UM HET3 from (BALB/cByJ _ C57BL/6J)F1 _ (C3H/HeJ _ DBA/2J)F1
老龄鼠应用研究
① 健康生命周期的基础生物学研究
② 骨质、肌肉、身体组成相关研究
③ 饮食、运动、认知与行为研究
④ 心血管、内分泌、代谢等疾病研究
⑤ 免疫学、肿瘤学、神经退行性疾病研究
⑥ 年龄相关的视力、听力障碍研究
百奥动物自主研发人源化小鼠模型、疾病模型、老龄鼠等上千种小鼠模型,欢迎来电咨询~
参考文献:
[1] Olshansky, S.J. From Lifespan to Healthspan. Jama 320, 1323-1324 (2018).
[2] Rivera-Tavarez, C.E. Can We Increase Our Health Span? Physical medicine and rehabilitation clinics of North America 28, 681-692 (2017).
[3] Beard, J.R. et al. The World report on ageing and health: a policy framework for healthy ageing. Lancet (London, England) 387, 2145-2154 (2016).
[4] Barzilai, N., Cuervo, A.M. & Austad, S. Aging as a Biological Target for Prevention and Therapy. Jama 320, 1321-1322 (2018).
[5]http://news.youth.cn/jsxw/202103/t20210310_12758403.htm
[6] J. Lustgarten.Cancer, aging and immunotherapy: lessons learned from animal models.Cancer Immunol Immunother 58:1979–1989(2009) .
[7] Mitchell, S.J., Scheibye-Knudsen, M., Longo, D.L. & de Cabo, R. Animal models of aging research: implications for human aging and age-related diseases. Annual review of animal biosciences 3, 283-303 (2015).
[8] Flurkey, K., M. Currer, J. & Harrison, D.E. Chapter 20 - Mouse Models in Aging Research. In: Fox, J.G. et al. (eds). The Mouse in Biomedical Research (Second Edition). Academic Press: Burlington pp 637-672(2007).
[9] https:// e. dxy. cn/ broadcast/ live/ id/ 22788/ ? source= wechat& sim= 1& sim_ token= jo3ALEk4m RZ9tfoghOHA rih1tV 6kp0IQvMAdhr7vws7ey9YqHi8uJxdmTk9vElaf
[10] C. F. Brayton, P. M. Treuting, and J. M. Ward.Pathobiology of Aging Mice and GEM: Background Strains and Experimental Design.Veterinary Pathology 49(1) 85-105(2012).

导读
动脉粥样硬化(atherosclerosis,AS)是一种缓慢型临床疾病,是心血管疾病的核心,是引起心肌梗死、中风和周围血管疾病的导火索[1]。脂质代谢异常造成的脂质沉积是动脉粥样硬化最直接的致病因素,受累动脉病变从内膜开始,积聚的脂质外观呈黄色粥样,一般先有脂质和复合糖类的异常沉积,进而纤维组织增生及钙质沉着,并伴随着动脉中层逐渐蜕变和钙化,导致动脉壁增厚变硬、失去弹性以及血管腔狭窄。
随着血管逐渐狭窄,病变又会累及不同器官,出现头晕、心痛、胸闷和顽固性高血压、糖尿病等症状,可以说动脉粥样硬化就像一颗“不定时炸弹”。目前我国是全球动脉粥样硬化疾病高发区,60岁以上老年人的发病率高达79.9%;并且近几年偏于年轻化趋势,严重影响人类的生命健康。

动脉粥样硬化及动脉斑块简图[2]
动脉粥样硬化是多因素共同作用引起的,发病机制较为复杂且尚未完全阐明。目前来看,大小鼠是动脉粥样硬化研究中最常用的物种,尽管有局限性,但其与人类的动脉粥样硬化过程的许多关键特征是相似的,仍然是动脉粥样硬化模型的首选物种。
动脉粥样硬化的发展与胆固醇运输颗粒低密度脂蛋白(LDL)密切相关[3],主要为载脂蛋白E(ApoE)基因和低密度脂蛋白受体(LDLR)基因,可为动脉粥样硬化的治疗和预防提供参考依据。
B-Apoe KO小鼠
载脂蛋白E(Apolipoprotein E, ApoE)是一种与脂质颗粒相关的载体蛋白,主要由肝脏和外周组织中的巨噬细胞产生,是血浆脂蛋白的核心成分。ApoE将脂蛋白、脂溶性维生素和胆固醇输送到淋巴系统,然后进入血液,防止富含胆固醇的颗粒在血浆中积聚,是预防、治疗动脉粥样硬化血管疾病的主要靶点基因。研究表明,ApoE能够通过多种方式预防动脉粥样硬化[4]:促进循环系统中富含甘油三酯的脂蛋白的有效吸收;维持正常的巨噬细胞脂质稳态;调节免疫功能等。
百奥动物BioMice利用基因编辑技术构建了B-Apoe KO小鼠。利用高脂饮食喂养诱导的小鼠胆固醇水平升高程度加大,硬块的形成进一步加剧,类似于人类动脉粥样硬化及动脉粥样硬化性心脏病中的饮食依赖性,可用于心血管疾病及阿尔兹海默症的研究。
B-Apoe KO小鼠特殊饮食诱导动脉粥样硬化模型的建立

(A-B)小鼠在12周和20周时的动脉粥样硬化斑块。(C-D)主动脉窦在第12周和第20周的油红结果。(E)12周时主动脉弓大体染色。

12周时动脉粥样硬化小鼠模型的组织染色和血液生化结果(A)主动脉窦的H&E结果增加。(B-C)免疫组化显示α-SMA和F4/80的表达。(D)血清ALT、AST、TC、TG、HDL-C和LDL-C水平。数值以平均值±SEM表示。**p<0.01,***p<0.001。
B-Ldlr KO大鼠
B-Ldlr KO大鼠的模型验证及分析

纯合Ldlrtm1/Bcgen大鼠在4个月大时表现出显著升高的血清胆固醇水平。
PCSK与动脉粥样硬化的关系
除了ApoE和LDLR基因外,还有其他与血脂调控相关的类似于PCSK9等靶点用于构建动脉粥样硬化模型,这些模型具有不同的致病机制和病理表型,助力动脉粥样硬化和高脂血症等疾病的研究及治疗药物的开发[6]。
PCSK9是近年来在降脂药开发领域研究的一个新兴靶点,主要在肝脏中表达。PCSK9在LDL-C代谢中发挥重要作用。在肝细胞质膜,分泌的PCSK9的催化结构域与LDL-R结合并被内化,进入内体途径。内体的低pH值增强了PCSK9对LDL-R的亲和力,防止受体再循环到细胞表面。而PCSK9与LDL-R结合后再与LDL-C结合形成新的复合体进入溶酶体中一起被降解,最终导致LDL-R 减少,LDL-C的降解随之减少,从而使LDL-C的水平升高[7]。

PCSK9 在 LDL 受体 (LDL-R) 代谢中的作用[7]
脂质代谢分析

B-hPCSK9 小鼠的脂质代谢分析。分析 B-hPCSK9 小鼠和野生型 C57BL/6 小鼠(n=36,6周)TG、TC、LDL-C和 HDL-C 的血浆浓度。B-hPCSK9小鼠和野生型 C57BL/6 小鼠之间无差异。TG:甘油三酯;TC:总胆固醇;HDL-C:高密度脂蛋白胆固醇;LDL-C:低密度脂蛋白胆固醇。
药效验证

抗人 PCSK9 抗体在 WD 诱导 B-hPCSK9 小鼠的体内有效性。B-hPCSK9 小鼠给予Alirocumab(内部)/Evolocumab(内部)或同型对照抗体(单次给药,s.c.)(n=8,雄鼠)。在第-5、1、3、5和8天采集血液进行分析。与同型对照相比,抗人 PCSK9 抗体给药组小鼠的血清 LDL-C(A) 和 TC(B) 水平降低,表明抗人 PCSK9 抗体可有效控制雄性 B-hPCSK9 小鼠的血脂。数值表示为平均值±SEM。TC:总胆固醇;LDL-C:低密度脂蛋白胆固醇。WD:西方饮食。

抗人 PCSK9 抗体上调 B-hPCSK9 小鼠的 LDLR 水平。B-hPCSK9 小鼠给予Alirocumab(内部)/Evolocumab(内部)或同型对照抗体(单次给药,s.c.)(n=6,雄鼠)。在第8天采集肝组织用于 ELISA 分析。与同种型对照相比,抗人 PCSK9 抗体给药组小鼠中 LDLR 水平上调。数值表示为平均值±SEM。LDLR:低密度脂蛋白胆固醇受体。WD:西方饮食。
表1. 动脉粥样硬化相关小鼠模型

参考文献
[1]Besa Emini Veseli,Paola PerrottaEuropean Journal of Pharmacology,Animal models of atherosclerosis,Volume 816, 5 December 2017.
[2]Wikipedia/CC BY 3.0
[3]Godfrey, S, Getz, Catherine, A, & Reardon. (2012). Animal models of atherosclerosis. Arteriosclerosis Thrombosis & Vascular Biology.
[4]Jean Davignon, Jeffrey S.Cohn, et al. Apolipoprotein E and atherosclerosis: insight from animal and human studies.Clinica Chimica Acta.Clinica Chimica Acta.
[5]Brown, Michael S, and Joseph L. Goldstein. A receptor-mediated pathway for cholesterol homeostasis. Science232.4746(1986): 34-47.
[6]Gresham, G. A. (2017). Animal models of atherosclerosis. Biomedical Reports, 6(3), 259-266.
[7]Hess, C. N., Low Wang, C. C. & Hiatt, W. R. PCSK9 Inhibitors: Mechanisms of Action, Metabolic Effects, and Clinical Outcomes. Annual review of medicine 69, 133-145
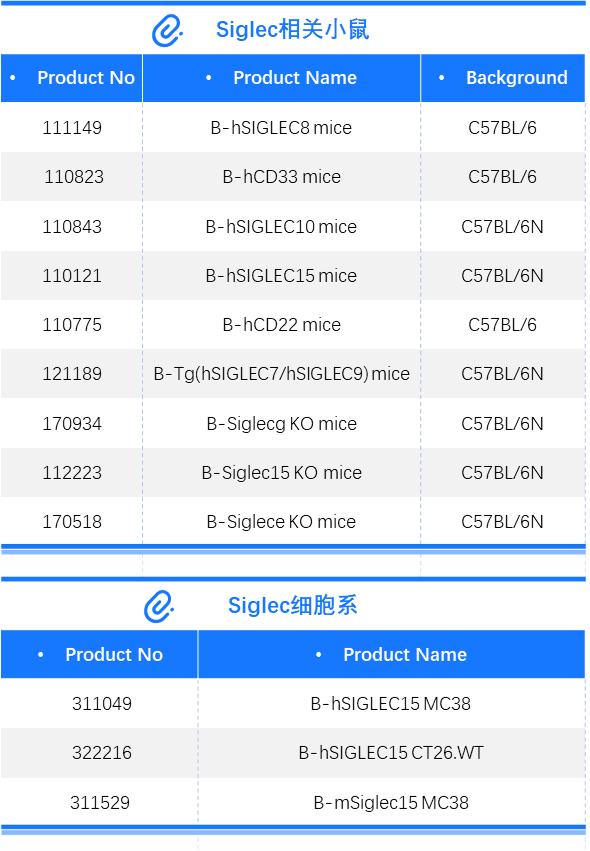
嗜酸性胃炎(EG)、嗜酸性十二指肠炎(EoD)和嗜酸性食管炎是一类严重的炎症性疾病,表现为胃、十二指肠和食管外嗜酸性粒细胞水平升高。目前没有针对此种疾病的有效疗法,采用全身性的类固醇激素疗法能够改善疾病症状,但长期使用会带来严重副作用。SIGLEC8因为具有强大的嗜酸性粒细胞促凋亡和肥大细胞抑制活性,并选择性表达在这些关键的炎症效应细胞的作用,被认为是很有前途的抗炎靶点。
靶点概述
Siglecs(结合唾液酸的免疫球蛋白型凝集素)是主要在造血系统细胞上发现的一类免疫调节受体。迄今为止,已在人类中鉴定出14种SIGLEC,主要在各种白细胞群上表达。[1]根据进化上的保守程度分为进化保守型和非保守型两类SIGLEC。保守型SIGLEC由SIGLEC1、SIGLEC2、SIGLEC4和SIGLEC15组成,它们在哺乳动物中存在直系同源基因;非保守型SIGLEC则由其他成员组成,在哺乳动物物种中并不存在真正的同源基因,被称为CD33相关基因 SIGLEC,其中就包括SIGIEC8。

图1. SIGLEC8促进嗜酸性粒细胞凋亡并减少肥大细胞炎症反应&SIGLEC8的潜在聚糖配体[2]
SIGLEC8是属于SIGLEC 家族 CD33样亚家族成员,全称为“sialic acid binding Ig like lectin 8”。它仅在人类嗜酸性粒细胞和肥大细胞上高度表达,在嗜碱性粒细胞上表达较弱。在体外,SIGLEC8在嗜酸性粒细胞上与抗体或合成聚糖配体包被的聚合物交联可诱导其快速凋亡,而在肥大细胞上,SIGLEC8 连接可抑制 IgE/FceRI介导的炎症介质释放,而不影响他们的生存[3]。用促进存活的促炎性细胞因子预激活嗜酸性粒细胞(过敏性炎症的一个关键过程)不仅不能抵消 SIGLEC8 触发的细胞死亡,反而会有效增强其对 SIGLEC8连接反应中细胞凋亡的敏感性,这表明SIGLEC8介导的免疫抑制在炎症条件下发挥着特殊作用,被认为是很有前途的抗炎靶点,因此在治疗过敏反应、哮喘等由这些细胞引发的炎症性疾病方面具有重要作用[4]。
新药研究进展
目前以SIGLEC8为靶点的在研药物共5项,开发机构均是Allakos。其中Antolimab(AK-002)处于临床II期,其余四项处于临床前阶段。Antolimab,是一款靶向SIGLEC8的人源重组非岩藻糖基化单克隆IgG1抗体的药物;能够通过SIGLEC8移植肥大细胞和消耗嗜酸性粒细胞,从而抑制有这两类细胞的错误激活导致的一系列疾病,如嗜酸性胃炎(EG)、嗜酸性十二指肠炎(EoD)和嗜酸性食管炎等慢性炎症疾病。2020年5月Allakos公布Antolimab在治疗EG、EoD和嗜酸性食管炎上已经获得了 FDA的孤儿药认定资格。

数据来源于科睿唯安
B-hSIGLEC8 mice
B-hSIGLEC8 小鼠中的嗜酸性粒细胞和肥大细胞与抗人 SIGLEC8 抗体结合

通过流式细胞术分析 B-hSIGLEC8 小鼠的嗜酸性粒细胞和肥大细胞。从野生型 C57BL/6 小鼠和B-hSIGLEC8小鼠中分离出嗜酸性粒细胞和腹膜灌洗肥大细胞。使用基准抗体 Lirentelimab(内部合成)进行流式细胞术分析以评估人 SIGLEC8 表达。Lirentelimab 在纯合 B-hSIGLEC8 小鼠中仅与 SIGLEC8结合,在野生型小鼠中不与 SIGLEC8结合。
小鼠哮喘模型BALF免疫细胞数量

从B-hSIGLEC8小鼠(n=6)中分离出BALF免疫细胞。在PBS或lirentelimab(内部合成)处理下,通过流式细胞术分析嗜酸性粒细胞的数量。lirentelimab 治疗后,纯合 B-hSIGLEC8 小鼠中炎症细胞的表达水平低于阳性对照。
抗人SIGLEC8抗体的药效

B-hSIGLEC8 小鼠哮喘样模型中的 H&E 染色。(A) 在研究结束时收集肺组织。H&E染色结果显示,暴露于PBS气雾剂的B-hSIGLEC8小鼠的肺组织没有表现出任何炎症。暴露于OVA导致 B-hSIGLEC8 小鼠的支气管周围和血管周围炎症显着增加。(B) 在用 lirentelimab(内部合成)治疗的小鼠中观察到嗜酸性粒细胞浸润显着减少。

本期分享到此结束,如果您对相关小鼠模型有需求,欢迎随时与我们联系。
参考文献
[1] Ravetch JV, Lanier LL (2000) Immune inhibitory receptors.Science290(5489):84–89.
[2] Angata T, Varki A. Discovery, classification, evolution and diversity of Siglecs. Mol Aspects Med. 2023 Apr;90:101117. doi: 10.1016/j.mam.2022.101117.Epub 2022 Aug 18. PMID: 35989204; PMCID: PMC9905256.
[3] Hudson SA, Bovin NV, Schnaar RL, Crocker PR, Bochner BS (2009) Eosinophil-selectivebinding and proapoptotic effect in vitro of a synthetic Siglec-8 ligand, polymeric6′-sulfated sialyl Lewis x.J Pharmacol Exp Ther330(2):608–612.
[4] Na HJ, Hudson SA, Bochner BS (2012) IL-33 enhances Siglec-8 mediated apoptosis ofhuman eosinophils.Cytokine57(1):169–174.

肿瘤相关髓系细胞(tumor-associated myeloid cells, TAMC)是肿瘤微环境(TME)中重要的组成部分,具有异质性,在肿瘤微环境中可以发挥不同,甚至是相反的作用,如免疫抑制或免疫刺激。靶向TAMCs作为单一疗法或与化疗、免疫疗法联合应用的研究正在火热进行中。深入研究TAMCs在肿瘤中的功能和作用机制将有助于发现新的治疗方法。 研究最多的肿瘤相关髓系细胞包括单核细胞、肿瘤相关巨噬细胞(TAMs)、树突状细胞(DC)、癌症相关循环中性粒细胞、肿瘤相关中性粒细胞(TANs)和骨髓来源抑制细胞(MDSCs)。TAMC的主要功能是调节淋巴细胞行为进而形成免疫刺激或免疫抑制性TME,从而抑制或促进包括肿瘤细胞的恶性克隆进化、生长、存活、侵袭、播散和转移、血管生成在内的各个肿瘤发展阶段。 单核细胞 单核细胞是一组异质性的单核吞噬细胞,分为经典型单核细胞、中间型单核细胞和非经典型单核细胞,在炎症期间循环外周血中发挥先天免疫功能。肿瘤发展的不同阶段,不同的单核细胞亚群表现出不同甚至相反的作用。 从机制上讲,中间型单核细胞经肿瘤细胞刺激后,促炎细胞因子TNF- α和白细胞介素12(IL-12)的产生增加,而抗炎细胞因子白细胞介素10(IL-10)的产生减少,并对肿瘤细胞产生直接的细胞毒性,促进肿瘤细胞凋亡。经典型单核细胞产生VEGF,促进肿瘤细胞外渗,导致转移。相比之下,非经典型单核细胞在吞噬肿瘤细胞衍生微粒后被激活,从而减少肿瘤细胞的转移。 肿瘤相关巨噬细胞(TAMs) 巨噬细胞作为单核吞噬细胞系统,在组织稳态和炎症中起着关键作用。巨噬细胞分为两个主要亚群,M1和M2巨噬细胞,在功能上是异质的。 M1巨噬细胞是对抗微生物感染的第一道防线,具有很强的抗原呈递能力诱导强烈的Th1反应。在脂多糖(LPS)、IFN-γ和粒细胞-巨噬细胞刺激因子(GM-CSF)的作用下,M1巨噬细胞经历经典激活,并优先分泌抗菌分子和促炎细胞因子。 M2巨噬细胞在限制免疫反应、诱导血管生成和组织修复方面起着关键作用。在白细胞介素4(IL-4)、白细胞介素13(IL- 13)、IL-10和CSF-1的作用下,M2巨噬细胞发生选择性激活并优先分泌抗炎细胞因子。 TAMs在肿瘤中的作用 树突状细胞(DC) DC在肿瘤中的作用 粒细胞 粒细胞可大致分为癌症相关循环中性粒细胞、肿瘤相关中性粒细胞(TANs)以及其他中性粒细胞。 癌症相关循环中性粒细胞 这些与癌症相关的循环中性粒细胞由功能异质性亚群组成,是循环外周血的多形核吞噬细胞,具有对抗微生物病原体的先天免疫功能。在癌症患者中,特别是在晚期和转移后,循环中性粒细胞数量增加,高中性粒细胞与淋巴细胞比率(NLR)与侵袭性癌症相关。 肿瘤相关中性粒细胞(TANs) 研究表明TME中的TANs可促进肿瘤细胞增殖、外渗和迁移,在肿瘤发展和转移中起着关键作用。TANs可释放弹性蛋白酶等颗粒内容物,促进肿瘤增殖和侵袭细胞;分泌IL-1β和MPPs促进肿瘤细胞外渗到转移前壁龛,从而促进癌细胞的扩散;激活TLR通路,促进肿瘤细胞的迁移、黏附、侵袭和转移。 除促肿瘤作用外,TANs还被证明通过产生ROS和TRAIL介导肿瘤细胞的细胞毒性。研究也表明TANs与TME中的淋巴细胞相互作用并调节其功能。 其他粒细胞 除了嗜中性粒细胞(neutrophilic),其他类型的粒细胞,如嗜酸性粒细胞(eosinophils)和嗜碱性粒细胞(basophils),对肿瘤也有影响。研究表明嗜酸性粒细胞具有抗肿瘤活性,对各种癌细胞都表现出直接的或间接的细胞毒性,从而抑制肿瘤生长。 中性粒细胞在肿瘤中的作用 骨髓来源抑制细胞(MDSCs) MDSCs是一组异质性的髓系祖细胞和处于不同发育阶段的未成熟髓系细胞,它们在血管中循环。在感染时,MDSCs迅速扩张并分化为粒细胞、单核细胞、巨噬细胞和树突状细胞,在调节免疫反应和组织修复中发挥重要作用。 肿瘤相关的MDSC由两个主要亚群体组成,粒细胞骨髓来源抑制细胞(GrMDSCs)和单核细胞骨髓来源抑制细胞(MoMDSCs)。GrMDSCs在表型和形态上与中性粒细胞相似,MoMDSCs在表型和形态上与单核细胞相似,研究表明GrMDSCs和MoMDSCs均参与T细胞介导的免疫抑制。 MDSCs及其亚群在肿瘤中的作用 髓系细胞在肿瘤免疫治疗的研究中的作用是毋庸置疑的,调节这些髓系细胞的发育、成熟和功能有助于发现新的肿瘤免疫治疗策略。然而,由于各种可互换亚群的复杂性和可塑性,这些髓系细胞执行重叠或相反的功能,目前控制TAMCs行为的分子机制在很大程度上尚不清楚。为进一步阐明髓系细胞各亚群在不同癌症中的功能,并确定其促肿瘤和抗肿瘤活性相关的分子机制,百奥动物自主研发一些列髓系靶点人源化小鼠,助力深入了解髓系细胞的复杂性,并设计新的肿瘤靶向治疗方法。 B-hTREM2 mice(C) 基本信息 体内药效 B-hCD36 mice 基本信息 体内药效 B-hPD-1/hPD-L1/hVSIR mice 基本信息 蛋白表达分析 髓系靶点人源化小鼠列表 参考资料: 1. Aixia Dou, Jing Fan. Heterogeneous Myeloid Cells in Tumors. Cancers (Basel). 2021 Aug; 13(15): 3772. 2. Sijin Cheng, Ziyi Li, et al. A pan-cancer single-cell transcriptional atlas of tumor infiltrating myeloid cells. Cell. 2021Feb; 184, 792–809. 肿瘤中单核细胞的功能
肿瘤中单核细胞的功能












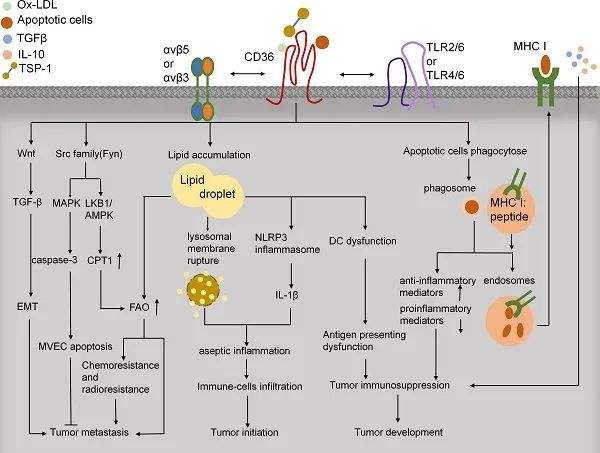
1973年,Kobylka和Carraway在乳腺上皮细胞中发现了一种在乳脂球中无法水解的膜蛋白,1978年,该分子被鉴定为血小板GPIV,一种介导血小板中血小板反应蛋白-1(TSP-1)结合的蛋白。随后,Tandon发现GPIV与白细胞分化抗原CD36具有重叠结构。随后,其他研究人员确定了CD36在血小板活化和细胞粘附中的作用。1993年,Abumrad及其同事证明了CD36的脂肪活性,之后将该蛋白在小鼠体内克隆并鉴定为人CD36的小鼠直系同源物,表明其在脂肪酸摄取中的作用。CD36现在被广泛认为是一种清道夫受体,可以吸收长链脂肪酸(LCFAs)和氧化低密度脂蛋白(ox-LDL)。 CD36是一种清道夫受体,在多种细胞类型中表达。在脂质代谢中发挥重要作用,介导脂质摄取、免疫识别、炎症、分子粘附和凋亡。与血管生成、炎症反应、动脉粥样硬化性血栓性疾病以及代谢紊乱性糖尿病和肥胖症等有关。在免疫系统中,CD36介导树突状细胞抗原的获取和呈递,并支持调节性T细胞功能。研究表明靶向CD36可能是提高CD8+T细胞免疫疗法的抗肿瘤药效的有效策略,为临床治疗提供了新的思路和可能。[1] CD36与PPAR-β激活[2] CD36靶向作用破坏肿瘤内Treg细胞,并启动PD-1阻断肿瘤。 具有抗CD36抗体的MOA: ①耗尽CD36+ Treg细胞。②阻断PPAR-和PPAR-依赖的代谢途径,降低线粒体活性和CD36表达水平,促进Treg细胞凋亡。③阻断TSP-1/CD36通路,促进TME血管生成。 CD36调节肿瘤免疫[3] CD36在肿瘤微环境中发挥作用。CD36调节下游Src家族激酶促进抗血管生成、FAO以及化疗耐药和放疗耐药,从而导致肿瘤转移。CD36还通过EMT激活Wnt/TGF-β信号传导促进肿瘤转移。CD36摄取多种脂质,如ox-LDL、LCFAs和胆固醇。免疫细胞中的脂质沉积导致树突状细胞的无菌性炎症和抗原呈递功能障碍,从而诱导肿瘤免疫抑制。此外,CD36可以与凋亡细胞结合并激活交叉引物,这可能导致免疫抑制和肿瘤发展。 BioMice百奥动物自主研发了人源化小鼠B-hCD36 mice和人源化细胞系B-hCD36 MC38助力科研。 B-hCD36 mice B-hCD36小鼠血常规检测 全血细胞计数(CBC)。采集雌性C57BL/6和B-hCD36小鼠(n=8,6-8周龄)的血液并进行全血细胞计数分析。B-hCD36小鼠的测量结果与C57BL/6小鼠相似,表明人源化不会改变血细胞组成和形态。数值表示为平均值±SEM。 B-hCD36小鼠血生化检测 B-hCD36小鼠的血生化试验。收集C57BL/6和B-hCD36小鼠(n=8,6-8周龄)的血清,并分析其指标水平。B-hCD36小鼠的测量结果与C57BL/6小鼠相似,表明人源化不会改变肝脏等相关组织的健康。数值表示为平均值±SEM。 使用抗CD36抗体测试B-hCD36模型的抗体结合试验 通过流式细胞术对纯合B-hCD36小鼠进行种属特异性CD36表达分析。收集野生型小鼠 (+/+)和纯合B-hCD36小鼠(H/H)的腹腔渗出巨噬细胞,并通过抗CD36抗体的流式细胞术进行分析。人CD36仅在纯合B-hCD36小鼠中可检测到,但在野生型小鼠中未检测到。CD36-1G04-hIgG1-LALA抗体在小鼠和人中交叉识别。 B-hCD36 MC38 蛋白表达分析 通过流式细胞术对B-hCD36 MC38细胞中的CD36表达进行分析。用种属特异性抗 CD36抗体对B-hCD36 MC38培养物的单细胞混悬液进行染色。在B-hCD36 MC38细胞表面检测到人CD36,但在野生型MC38细胞表面未检测到。使用B-hCD36 MC38细胞的10-G12克隆进行体内实验。 肿瘤生长曲线和体重变化 B-hCD36 MC38细胞的皮下同种移植肿瘤生长。将B-hCD36 MC38细胞(5x105)和野生型MC38细胞(5x105)皮下植入B-hCD36小鼠(雌性,7周龄,n=5)。每周测量两次肿瘤体积和体重。(A)平均肿瘤体积±SEM。(B)体重(平均值±SEM)。体积以mm3表示,使用公式:V=0.5X长径X短径2。如图A所示,B-hCD36 MC38细胞能够在体内建立肿瘤,可用于有效性研究。 肿瘤细胞蛋白表达分析 将B-hCD36 MC38细胞皮下移植到B-hCD36小鼠(n=5)中,接种后35天,收获肿瘤细胞并通过流式细胞术评估人CD36表达。如图所示,人CD36在肿瘤细胞表面高度表达。因此,B-hCD36 MC38细胞可用于新型CD36疗法的体内药效研究。 更多验证数据信息,正在研究进行中,敬请关注。想要获取更多百奥动物自主研发的人源化小鼠信息,请访问百奥动物官网或扫描下方二维码。 参考文献 1.CD36-mediated ferroptosis dampens intratumoral CD8+T cell effector function and impairs their antitumor ability 2.Wang, H., Franco, F., Tsui, Y. et al. CD36-mediated metabolic adaptation supports regulatory T cell survival and function in tumors. Nat Immunol 21, 298–308 (2020). doi:10.1038/s41590-019-0589-5 3.Wang, Jingchun; Li, Yongsheng (2019). CD36 tango in cancer: signaling pathways and functions. Theranostics, 9(17), 4893–4908. doi:10.7150/thno.36037 







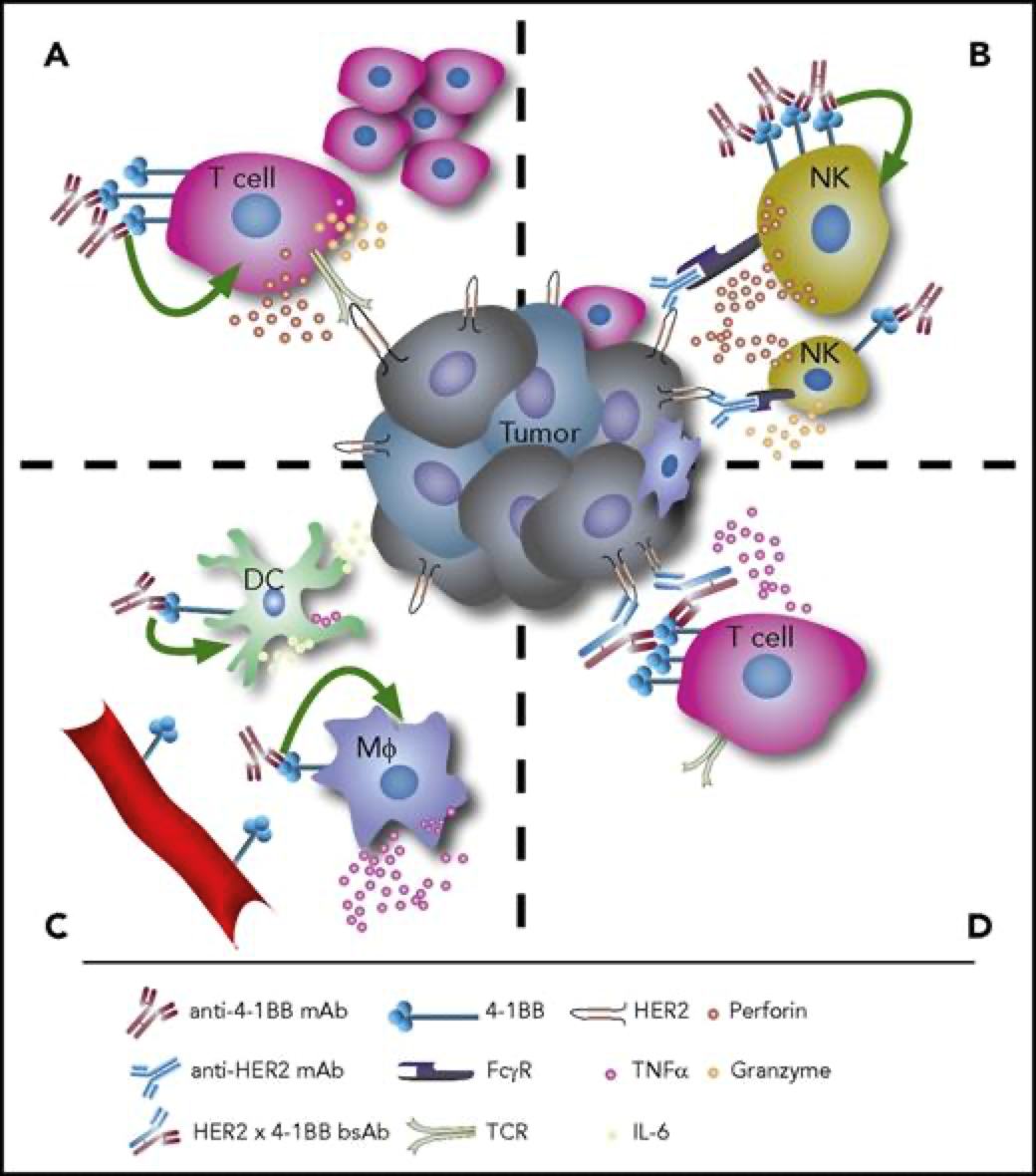
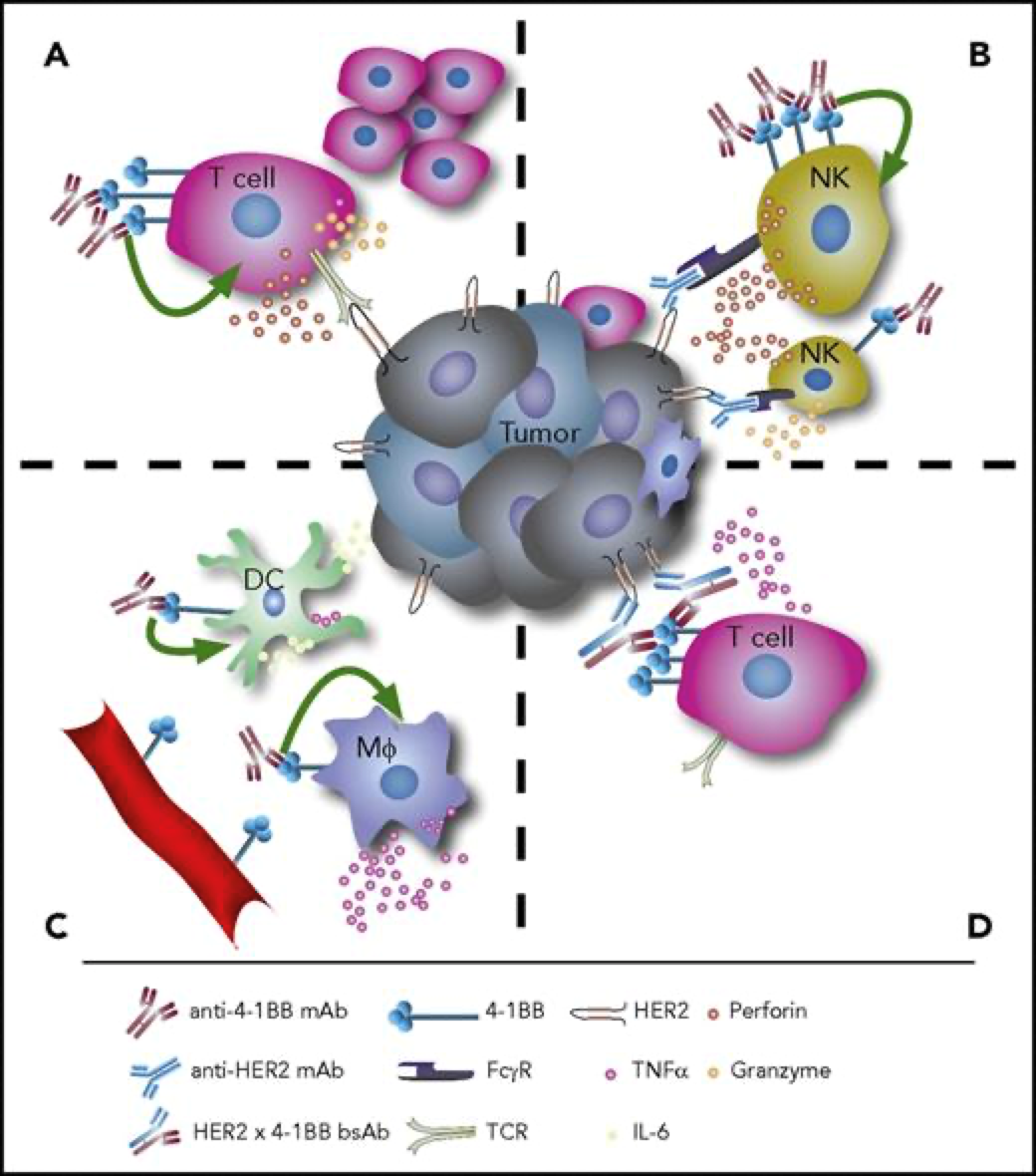
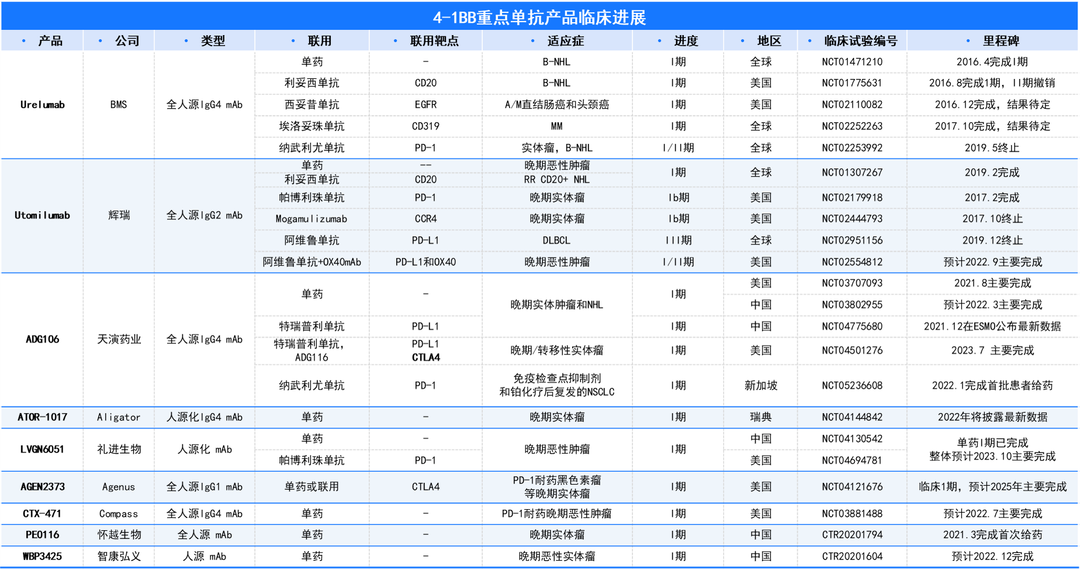
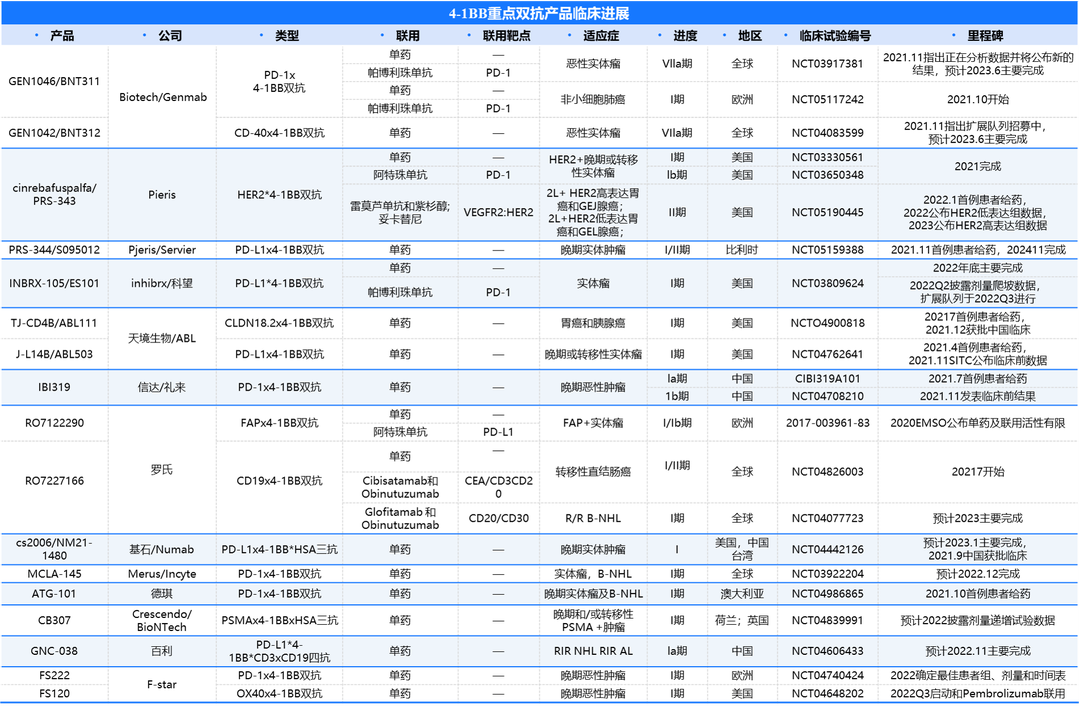
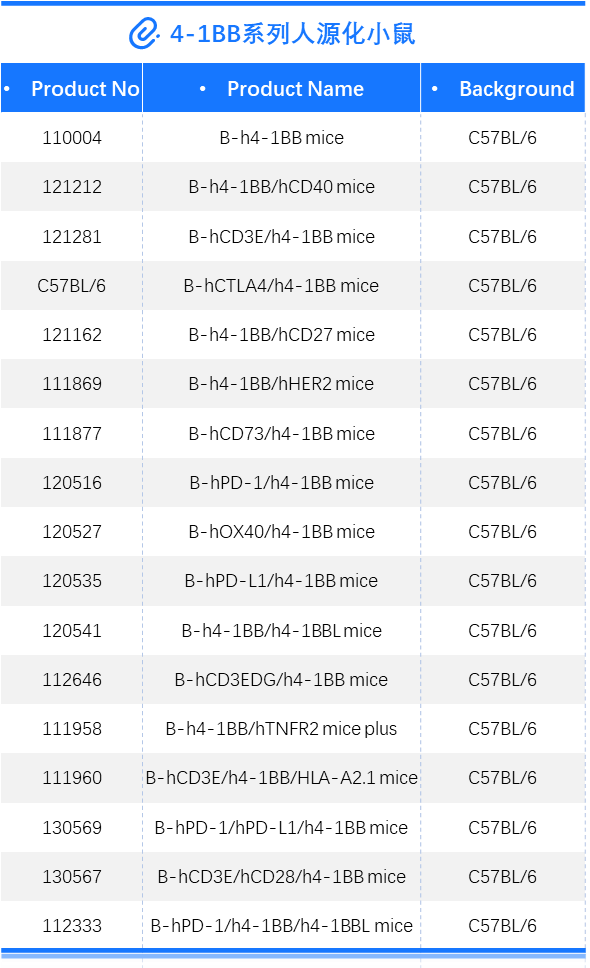
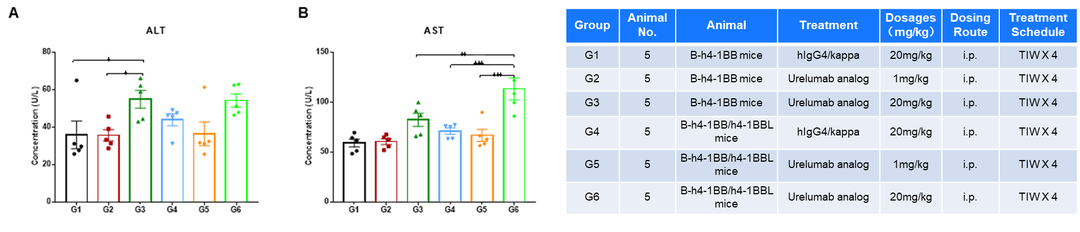
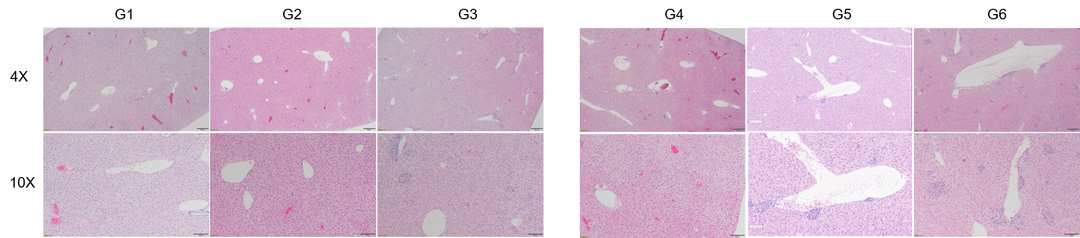
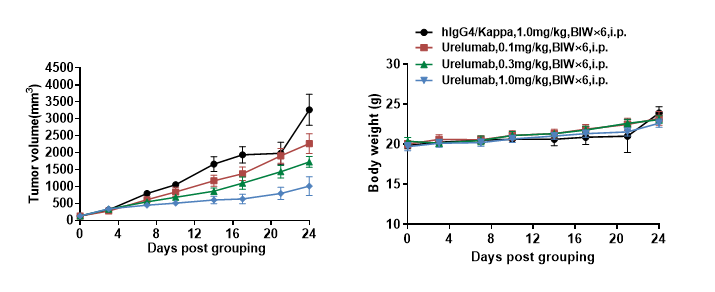
4-1BB靶点介绍 4-1BB,即CD137,TNFRSF9(TNF receptor superfamily member 9),它于1989年首次被发现,属于TNF受体超家族。它在抗原启动的T细胞上表达,在静止的T细胞上不表达,除此以外,4-1BB还在树突状细胞(DC)、自然杀伤细胞(NKs)、活化的CD4+和CD8+T淋巴细胞、嗜酸性粒细胞、自然杀伤T细胞(NKT)和肥大细胞中表达。 当4-1BB与其配体4-1BBL结合后,可以产生共刺激信号诱导CD4+和CD8+T细胞的活性,促进T细胞增殖,刺激巨噬细胞产生如如IL-6、TNF-α等多种炎症细胞因子。从而激活机体免疫系统,达到抑制肿瘤发生发展、促进肿瘤细胞清除的功效。 有研究报道,当在进行4-1BB抗体药物研发时,还要需要考虑抗体结合位点在人和小鼠之间存在的差异性。其结合作用仅限于富含半胱氨酸结构域(CRD),小鼠4-1BBL主要与CRDII结合,人4-1BBL主要与CRDIII结合。小鼠4-1BB/4-1BBL是二聚体,人4-1BB/4-1BBL为三聚体,且人4-1BB不与小鼠的4-1BBL相互作用。[1] 图1. 抗4-1BB疗法的免疫调节作用[2] 4-1BB药物开发的现状 4-1BB作为癌症免疫疗法中十分有潜力的靶点,针对其进行的药物研发非常火热,全球目前已有至少40款4-1BB激动型抗体进入临床研究阶段。 4-1BB单抗药物 由 BMS研发的Urelumab(全人源IgG4 mAb)是一个4-1BB强激动性的单抗,在I/II期试验中表现出良好的抗肿瘤活性,但在后续治疗过程中发生了两起由肝毒性引起的致命性不良事件。由Pfizer研发的Utomilumab(人源化IgG2 mAb)是一个4-1BB弱激动性的单抗,虽然有较好的肝脏安全性表现,但作为单药治疗抗肿瘤活性十分有限。 因此,此前未能很好的在激动作用和肝毒性之间达到良好的平衡,导致4-1BB单抗产品临床应用空间有限;目前新一代单抗设计通过对Fc功能改造试图保留激动性的同时克服安全性问题,Alligator、Agenus以及国内的礼进生物和天演药业的4-1BB单抗产品表现出良好的初步临床数据。 4-1BB重点单抗产品临床进度 数据来源:Cortellis 4-1BB双抗药物 平衡抗体激动作用强弱和其肝毒性,是4-1BB单抗药物开发的难点,因此为了克服疗效和毒性的问题,研究者们开始探索新的开发策略。其中以4-1BB为靶点的双抗、三抗以及四抗成为研发的一个热点领域,国内外多家药企均有布局。 4-1BB双特异性抗体通过对肿瘤细胞表面靶点和4-1BB亲和力不同精准定位肿瘤微环境,减少肝毒性等副作用。因此双抗疗效相比单抗可以实现更精准的靶向,从而使得临床前的抗肿瘤活性和安全性都得到了提升。 如PD-1/PD-L1就是4-1BB双抗常用的另一候选靶点。去年,BioNTech与Genmab联合研发的PD-L1×4-BB双抗药物GEN1046,是一种全长IgG1亚型的PD-L1×4-1BB双抗,其以临床Ⅰ/Ⅱa期结果发表在著名学术期刊《CANCER DISCOVERY》上的文章中,所使用的PD-L1/4-1BB双靶点人源化鼠由百奥动物提供。文中研究结果表明:GEN1046对于CPI耐药的实体瘤治疗效果良好,安全性高,为免疫联合治疗提供了新的方案。 4-1BB重点双抗产品临床进度 数据来源:Cortellis 通过众多临床试验及以往多年研究积累,4-1BB 靶点被证实是肿瘤免疫治疗十分有潜力的靶点,目前如何最大化激动作用并最小化毒性是未来4-1BB激动剂研发亟需解决的问题。百奥动物自主研发的4-1BB系列人源化小鼠(详情见下表),是靶向4-1BB抗体开发相关药物进行药效评价的优质模型。 B-h4-1BB/h4-1BBL mice 高剂量Urelumab对B-h4-1BB小鼠和B-h4-1BB/h4-1BBL小鼠均产生肝毒性 用PBS或Urelumab(内部合成)对纯合子B-h4-1BB小鼠和B-h4-1BB/h4-1BBL小鼠进行治疗 (n=5,雌性,7周龄)。第21天采集血清,检测谷丙转氨酶(ALT)、谷草转氨酶(AST)。与PBS对照相比,使用20mg /kg Urelumab治疗B-h4-1BB小鼠的ALT显著升高,而同样的治疗对B-h4-1BB/h4-1BBL小鼠没有影响。与PBS对照相比,B-h4-1BB小鼠AST无明显升高,但20ug/mL urelumab治疗可使B-h4-1BB/h4-1BBL小鼠AST明显升高。在1mg/kg剂量组,B-h4-1BB小鼠和B-h4-1BB/h4-1BBL小鼠的ALT和AST均无明显变化。表明高剂量urelumab对B-h4-1BB和B-h4-1BB/h4-1BBL小鼠有肝毒性作用。数值以平均值±SEM表示。 高剂量Urelumab 治疗可导致B-h4-1BB小鼠和B-h4-1BB/h4-1BBL小鼠肝脏淋巴细胞浸润增加 肝毒性的病理分析。在B-h4-1BB小鼠(G1-G3)中,当urelumab剂量为1mg/kg时,肝脏未见明显异常变化(G2)。当剂量为20 mg/kg (G3)时,观察到血管周围细胞浸润或肝脏慢性炎症,并伴有轻度病变。 在B-h4-1BB/h4-1BBL小鼠(G4-G6)中,1 mg/kg组(G5) 3/5的小鼠出现病理变化(轻度2/5,轻度1/5),而在20 mg/kg剂量(G6)时,所有实验动物肝脏均出现中度变化。总体而言,20 mg/kg组(G6)肝脏病变程度和发生率显著高于1 mg/kg组(G5)。 以上结果提示,高剂量(20mg /kg)的urelumab比低剂量(1mg /kg)的urelumab更容易发生血管周围细胞浸润或肝脏慢性炎症。B-h4-1BB/h4-1BBL小鼠对urelumab毒性作用比B-h4-1BB小鼠更敏感。因此B-h4-1BB/h4-1BBL小鼠是较好的临床前毒性评价模型。 B-h4-1BB/h4-1BBL药效验证 抗人4-1BB抗体在B-h4-1BB/h4-1BBL小鼠中的抗肿瘤药效。(A) 纯合子B-h4-1BB/h4-1BBL小鼠 (雌性,6-8周龄,n=5) 皮下接种小鼠结肠癌MC38细胞系。结果显示抗人4-1BB抗体能够显著抑制MC38肿瘤细胞的生长。(B)治疗期间体重变化。如图A所示,抗人4-1BB抗体在B-h4-1BB/h4-1BBL小鼠中有效地控制肿瘤生长,这表明B-h4-1BB/h4-1BBL小鼠可为体内评价抗人4-1BB抗体药效提供有力的临床前研究模型。值表示为平均值±SEM。 参考文献 [1].https://mp.weixin.qq.com/s/kvwfybpx63XQn26xdijIZw https://mp.weixin.qq.com/s/999cX0RaXHLyXxZ8MhIaBw [2]. Chester C, Sanmamed MF, Wang J, Melero I. Immunotherapy targeting 4-1BB:mechanistic rationale, clinical results, and future strategies. Blood. 2018 Jan4;131(1):49-57. doi: 10.1182/blood-2017-06-741041. Epub 2017 Nov 8. PMID:29118009.