| 概述 | 阿普斯特( apremilast)由美国Celgene 生物技术公司开发,2014年3月21日经美国食品药品监督管理局(FDA)批准用于成人活跃型银屑病性关节炎(PsA)的治疗。 |
| 药品概况 | 名称:阿普斯特 别名:N/A,CC-10004
英文名:apremilast
商品名:Otezla
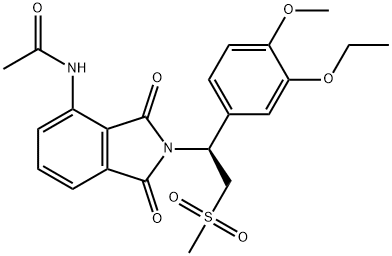
中文名称:S)-2-[1-(3-乙氧基-4-甲氧基苯基)-2-甲磺酰基乙基]-4-乙酰基氨基异吲哚啉-1,3-二酮
英文化学名:(+)-N-[2-[1(S)-(3-ethoxy-4-methoxyphenyl)-2-(methylsulfonyl) ethyl]-1,3-dioxo-2,3-dihydro-1H-isoindol-4-yl]acetamide
分子式:C22H24N2O7S
分子量:460.5
CAS号:608141-41-9
原研公司:Celgene 公司
药理分类:磷酸二酯酶-4(PDE-4)和肿瘤坏死因子-α(TNF-α)双重抑制剂
适应症:银屑病、银屑病关节炎
目前阶段:III 期临床
给药途径:口服
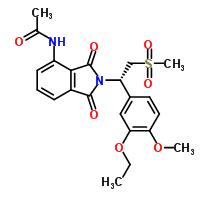
图1-阿普斯特的结构式 |
| 银屑病治疗药物 | 阿普斯特(apremilast)是由美国Celgene公司研发的一种口服、选择性磷酸二酯酶4(PDE4)抑制剂,商品名称Otezla,该药是FDA批准的首个也是唯一一个用于斑块型银屑病治疗的PDE4抑制剂,用于适合光疗和系统疗法的中度至重度斑块型银屑病(Plaque Psoriasis)成人患者的治疗。
2014年3月21日,美国FDA批准Otezla (apremilast)用于治疗活跃型银屑病性关节炎(PsA)成人患者。大多数人先出现银屑病,而后被诊断患有PsA。关节疼痛、僵硬和肿胀是PsA的主要体征和症状。目前被批准用于PsA的药物有糖皮质激素、肿瘤坏死因子(TNF)阻断剂及白介素-12/白介素-23抑制剂。
Otezla是一种磷酸二酯酶-4(PDE-4)抑制剂,其安全性及有效性基于三项由1493名活跃型银屑病性关节炎患者参与的3期临床试验。Otezla治疗患者与安慰剂患者相比,其PsA体征及症状显示有改善,apremilast组与安慰剂组的ACR20应答率分别为32-41%、18-19%。阿普斯特是一个全新作用机制的口服抗风湿药物,与目前临床常用的anti-TNF单抗有区别,EvaluatePharma预测2018年销售额为12.19亿美元。
Otezla治疗患者应定期让卫生保健专业人员监测其体重。如果出现无法解释或临床上明显的体重减轻,应对体重减轻进行评价,并应考虑中止治疗。Otezla治疗患者与安慰剂患者相比,抑郁症风险有所增加。
在临床试验中,Otezla用药患者最常见的副作用有腹泻、恶心和头痛。Otezla由位于新泽西班州Summit的塞尔基因公司生产。
图1为美国Celgene公司生产的阿普斯特片(商品名称:Otezla)。 |
| 临床前研究 | 1、体内活性研究
首先把正常人的皮肤移植到米色严重联合免疫缺陷(SCID)小鼠的身上,移植4周后,以银屑病病人的自然杀伤细胞(NK细胞)来刺激皮肤。注射NK细胞两周后,把小鼠分为3组,每组7只,分别经口服给予阿普司特、环孢霉素安慰剂。阿普司特组和环孢素组在组织学特征上有部分或完全恢复的比率分别为57.1%、42.9%。结果表明本药品能有效地减少表皮厚度,同时能有效降低TNF-α、细胞内黏附分子-1(ICAM-1)和人类白细胞抗原DR(HLA-DR)等炎症相关物质的浓度,其药效作用优于环孢素组。
2、药动学
患者po阿普司特20 mg/d,观察29 d的药动学参数。半衰期(t1/2)为 8.2 h,药时曲线下面积为 1.799μg/mL,血浆药物达峰时间(tmax)为 2 h,生物利用度为 10.4 L/h,分布容积为 128 L,平均稳态的血浆最大浓度(Cmax)为 0.207 μg/mL(0.450 μmol/L),该浓度下阿普司特能有效抑制约 70%由外周血单核细胞(PBMC)诱导的脂多糖(LPS)所产的THF-α。 |
| 临床评价 | 与同类药物相比阿普斯特(商品名称:Otezla)具有以下优势:
1、它可抑制多种促炎症介质(PDE-4、TNF-α、IL-2、干扰素r、白三烯、NO 合成酶)的生成而发挥抗炎作用。
2、磷酸二脂酶4(PDE4)选择性抑制剂,除批准用于银屑病性关节炎外,2014年9月FDA批准用于光疗或全身疗法的中重度治疗斑块状银屑病患者。是首个也是唯一获准用于治疗斑块状银屑病的PDE4抑制剂。
3、临床试验显示,阿普斯特可减少中重度斑块状银屑病患者的红斑、增厚和脱屑。
4、临床试验证明阿普斯特耐受性好,不良反应较小,临床试验中Otezla治疗组与安慰剂比较,患者显示PsA体征和症状的改善,包括触痛、关节肿胀和身体功能。
5、其他适应症正在做临床,如风湿性关节炎、强制性脊髓炎、白塞氏病、溃疡性结肠炎等。市场潜力较大。 【注册分类】按照注册管理方法的要求,原料为3.1类,片剂为3.1。
【剂型及规格】原料及片剂,10mg,20mg,30mg。
【适应症】适用于为治疗有活动性银屑病关节炎的成年患者。
本信息由Chemicalbook晓楠编辑(2015-08-14)。 |
| 阿普斯特相关专利信息 | 阿普斯特相关专利信息:
化合物:WO0025777,国内无专利。
用途:ZL03811093.8/ZL200610137407.4,2023.03.20。
晶型:CN200880129462.6,2008.03.27。 |
| 制备方法 | 1、以3-乙氧基-4-甲氧基苯甲腈(1)为原料,在四氢呋喃中与二甲基亚砜(在四氢呋喃中经正丁基锂预处理)反应得到烯胺衍生物(2),随后在三氟乙醇溶液中于50 ℃下经不对称氢化还原得到所需的S型胺(3)。向3的甲醇溶液中加入N-乙酰-L-亮氨酸得到对应的盐(4),最后与苯并呋喃衍生物(5)在乙酸中回流,经缩合反应得到阿普斯特。5可由3-硝基邻苯二甲酸经硝基还原后,再与乙酸酐发生酰化反应制得。合成路线如下:

2、以3-乙氧基-4-甲氧基苯甲醛为原料,在六甲基二硅胺基锂四氢呋喃溶液中生成3-乙氧基-4-甲氧基苯甲醛的亚胺,再与二甲基砜、正丁基锂和三氟化硼的乙醚溶液在78℃下反应得到 1-(3-乙氧基-4-甲氧基-苯基)-2-甲磺酰基-乙酮(1);甲醇为溶剂,化合物1与N-乙酰-L-亮氨酸经化学拆分得到S型异构体化合物(2);化合物2与3-N-乙酰氨基邻苯二甲酸酐在醋酸中回流,经缩合反应得到目标化合物阿普司特
。合成路线如下:
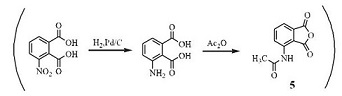 |
| 作用机制 | 本品特异性地以PDE-4为靶点来调控先天免疫细胞中促炎和抗炎介质的表达。在单核细胞核树突细胞中,来源于Toll样受体(TLR4)途径的促炎信号会引起转录核因子kappa B(NF-κB)的激活以及促炎介质的表达,如IL-23、TNF-α 和IFN-g。来源于G蛋白偶联受体(GPCRs)如前列腺素结合蛋白的信号通过刺激G蛋白α亚基(Gas)来激活腺苷酸环化酶(AC),从而产生cAMP。在白细胞如巨噬细胞和树突细胞中,cAMP会被PDE-4水解成AMP。阿普司特作为 PDE-4 的抑制剂能增加细胞内cAMP的水平,从而激活cAMP 依赖性蛋白激酶A(PKA),同时激活环核苷酸–门控离子通道,PKA的活化导致转录因子中cAMP反应元件(CRE)结合家族的磷酸化,同时激活转录因子1(ATF-1)。在特定细胞如巨噬细胞中,这些因子如IL-10会结合到CRE基因启动子的结合位点上增加细胞基因的表达,CRE 驱动的转录激活会集合共激活因子如CREB结合蛋白(CBP)、同源蛋白p300等。从NF-κB集合来的CBP 和p300会抑制NF-κB 的转录活性降低NF-κB依赖性基因的表达,从而导致IL-23、TNF-α和 IFN-g的降低。炎症反应的应答降低会使免疫细胞的炎性浸润降低,同时减少角质形成细胞和滑膜细胞的增殖激活,降低银屑病的表皮增厚以及关节炎中的滑膜损害。 |
| 安全性 | 1、抑郁
使用本品治疗时,发生抑郁的不良反应与其剂量增加有相关性。因此,有抑郁和/或自杀想法或行为史的患者使用本品前应仔细权衡治疗风险和获益。对患者、护理人员和家属应告知需警戒抑郁、自杀想法或其他情绪变化的出现或恶化;如果有此类情况发生,应及时处理并仔细评价是否继续使用本品。
2、体重减轻
使用本品治疗的患者应定期监测体重,如发生不能解释或临床意义的体重减轻,应进行评价,并考虑终止应用本品。
3、不良反应
常见的不良反应有恶心、腹泻、头痛、上呼吸道感染、鼻咽炎和上腹痛等,绝大多数属轻度或中度,大多在4周内消失。 |
| 生物活性 | Apremilast (CC-10004)是一种口服生物有效的PDE4和TNF-α抑制剂,IC50分别为74 nM和77 nM。 |
| 体外研究 | Apremilast抑制PDE4比其他PDE家族的cAMP 或cGMP水解酶更有效。Apremilast作用于多种类型的细胞,具有广泛的抗炎活性,抑制TNF-α,IL-12和IL-23的产量,及NK和角质形成细胞的反应。Apremilast抑制IL-8中酵母多糖诱导的PMN产生,IC50为94 nM。Apremilast 抑制fMLF诱导的PMN CD18 和CD11b表达,IC50分别为390 nM 和 74 nM, 且抑制fMLF诱导的PMN与HUVECs 粘连,IC50 为150 nM。Apremilast 抑制角质形成细胞TNF-α的产生, 通过测量细胞内ATP水平发现Apremilast对角质形成细胞存活力没有影响。 |
| 体内研究 | 在有人类微粒体(t1/2>60 min)存在时,Apremilast是稳定的。90%蛋白在人体血浆中结合。口服和静脉给药雌性大鼠,显示Apremilast具有良好的药代动力学,低清除力,适中的容积分布,口服生物利用度为64%。Apremilast在体内处理LPS诱导的TNF-α抑制大鼠模型,检测Apremilast抑制TNF-α的能力,测定ED50为0.03 mg/kg。Apremilast处理另一个LPS诱导的中性粒细胞大鼠模型,ED50为0.3 mg/kg 到 0.9 mg/kg。 |
| 药物相互作用 | 1、阿普斯特不是有机阴离子转运蛋白(OAT)1,OAT3,OCT2以及有机阴离子转运多肽(OATP)1B1和OATP1B3或乳癌耐药蛋白(BCRP)的抑制剂。
2、在体外,阿普斯特虽然是一种P-糖蛋白(P-gp)的底物,但在体内的生物利用度>70%,与酮康唑(DDI研究CYP3A和P-gp抑制剂) 未发现有显著的相互作用。因此,不会抑制P-gp的全身浓度。
3、阿普斯特(30 mg,qd,po)与口服避孕药、酮康唑或氨甲蝶呤同时服用,尚未观察到显著药动学相互作用。
4、CYP 450诱导剂利福平(600 mg,qd,po,共 15 d)与阿普斯特(30 mg,qd,po)同时服用,结果导致阿普斯特的AUC和Cmax分别降低 72%和 43%。 |
| 参考资料 | [1] 陈建超编译. 阿普斯特( apremilast). 中国药物化学杂志. 2014. 24(5).
[2] 赵倩, 孙悦, 石玉,等. 磷酸二酯酶-4抑制剂阿普司特[J]. 现代药物与临床, 2014, 29(4): 428-433.
[3] 吴爱萍,张志叶,王莉. 治疗银屑病关节炎新药阿普斯特的药理作用及临床评价. 新药述评与论坛.
中国新药杂志 2015, 24 (9).
说明:所给资料有限,主要总结了其制备方法、药理作用机理及其安全性方面的文献,为其在医药方面的应用打下基础。 |
| 用途 | 适用于为治疗有活动性银屑病关节炎的成年患者。 |
![S)-2-[1-(3-乙氧基-4-甲氧基苯基)-2-甲磺酰基乙基]-4-乙酰基氨基异吲哚啉-1,3-二酮](http://shop-files.yaozh.com/596793/5e9b2bdfc5510d22f9c5dabdbdbd7690.jpg_f.jpg)