
药品名称呋喃西林
外文名Nitrofural(Nitrofurazone)
主要适用症消毒防腐药
用法用量局部外用
分子式C6H6N4O4
分子量198.136
外观淡黄色结晶性粉末
熔点242至244℃
沸点335.4℃
闪点2℃
CAS登录号59-87-0
EINECS登录号200-443-1
安全性描述S26;S36/37
危险性符号Xn
危险性描述R22
呋喃西林,是一种用作消毒防腐药的有机化合物,化学式为C6H6N4O4,在临床上用于治疗创伤、烧伤、化脓性皮炎、中耳炎、泪囊炎、阴道炎、膀胱冲洗、褥疮等。
2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,呋喃西林在3类致癌物清单中。[3]
2019年12月27日,呋喃西林被列入食品动物中禁止使用的药品及其他化合物清单。
适应症
临床仅用作消毒防腐药,用于皮肤及粘膜的感染,如化脓性中耳炎、化脓性皮炎、急慢性鼻炎、烧伤、溃疡等。对组织几乎无刺激,脓、血对其消毒作用无明显影响。
药理作用
呋喃西林能干扰细菌的糖代谢过程和氧化酶系统而发挥抑菌或杀菌作用,主要干扰细菌糖代谢的早期阶段,导致细菌代谢紊乱而死亡。其抗菌谱较广,对多种革兰阳性和阴性菌有抗菌作用,对厌氧菌也有作用,对绿脓杆菌和肺炎双球菌力弱,对假单孢菌属及变形杆菌属有耐药性,对真菌,霉菌无效,但对因霉菌引起的细菌感染仍有相当效力。对敏感菌的杀菌浓度为13~20μg/mL,抑菌浓度为5~10μg/mL。

愈创木酚磺酸钾,用途是刺激性祛痰药,用于慢性支气管炎、支气管扩张的治疗等。
中文名愈创木酚磺酸钾
外文名guaiacolsulfonicacidpotassium
别名知阿可尔
中文别名知阿可尔
CAS号1321-14-8
EINECS号215-314-5
分子式C7H7KO5S
分子量242.2908
性状:白色结晶粉末。
生态学数据
对是水稍微有危害的不要让未稀释或大量的产品接触地下水、水道或者污水系统,若无政府许可,勿将材料排入周围环境。
性质与稳定性
如果遵照规格使用和储存则不会分解,未有已知危险反应,避免氧化物
用途
刺激性祛痰药,促进支气管分泌,使痰液变稀易于咳出。尚有微弱抗炎作用,用于慢性支气管炎、支气管扩张等。
贮存方法
保持贮藏器密封、储存在阴凉、干燥的地方,确保工作间有良好的通风或排气装置
药物信息
性状:糖浆剂。
用法及用量:口服。每次0.1~1g,每日3次。

氟马西尼
Fumaxini
Flumazenil
本品为8-氟-5,6-二氢-5-甲基-6-氧代-4H-咪唑并-[1,5-α][1,4]苯并二氮䓬-3-甲酸乙酯。按干燥品计算,含C15H14FN3O3不得少于99.0%。
【性状】本品为白色或类白色结晶性粉末;无臭。
本品在三氯甲烷或冰醋酸中易溶,在甲醇中略溶,在水中几乎不溶。
熔点本品的熔点(通则0612第一法)为198~202℃,熔融时同时分解。
【鉴别】(1)取本品约10mg,滴加冰醋酸使恰能溶解,加稀碘化铋钾试液,即生成橙红色沉淀。
(2)取本品,加甲醇溶解并稀释制成每1ml中含4μg的溶液,照紫外-可见分光光度法(通则0401)测定,在244nm的波长处有最大吸收,在227nm的波长处有最小吸收。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集993图)一致。
(4)本品显有机氟化物的鉴别反应(通则0301)。
【检查】醋酸溶液的澄清度与颜色取本品0.10g,加醋酸10ml溶解后,溶液应澄清无色。
有关物质照高效液相色谱法(通则0512)测定。
供试品溶液取本品,加流动相溶解并稀释制成每1ml中含1.0mg的溶液。
对照溶液精密量取供试品溶液适量,加流动相定量稀释制成每1ml中含10μg的溶液。
色谱条件用十八烷基硅烷键合硅胶为填充剂;以稀磷酸溶液(取水1000ml,用磷酸调节pH值至2.0)-甲醇-四氢呋喃(80∶13∶7)为流动相;检测波长为230nm;进样体积20μl。

南昌白云硫酸镁原料药有GMP资质批文
南昌白云硫酸镁原料药有GMP资质批文
MgSO4•7H2O 246.48
本品按炽灼至恒重后计算,含MgSO4不得少于99.5%。
【性状】本品为无色结晶;无臭;有风化性。
本品在水中易溶,在乙醇中几乎不溶。
【类别】泻药、利胆药。
【贮藏】密封保存。
【制剂】硫酸镁注射液
七水硫酸镁,又名硫苦、苦盐、泻利盐、泻盐, 化学式为MgSO4·7H2O),为白色或无色的针状或斜柱状结晶体,无臭,凉并微苦。受热分解,逐渐脱去结晶水变为无水硫酸镁。医药上用作泻盐。
中文名七水硫酸镁 [1] 外文名magnesium sulfate heptahydrate [1] 别 名硫苦;苦盐;泻利盐;泻盐化学式MgSO4·7H2O分子量246.47CAS登录号10034-99-8


维生素D2厂家,药用维生素D2批发,维生素D2价格,维生素D2医药级,维生素D2药用级,维生素D2国药准字号原料,cp2020标准维生素D2 本品为9,10-开环麦角甾-5,7,10(19),22-四烯-3β-醇。含C28H44O应为97.0%~103.0%。 【性状】 本品为无色针状结晶或白色结晶性粉末;无臭;遇光或空气均易变质。 本品在三氯甲烷中极易溶解,在乙醇、丙酮或乙醚中易溶,在植物油中略溶,在水中不溶。 本公司主营 醋酸氯己定 舒巴坦钠 羊毛脂 醋酸地塞米松 薄荷脑 薄荷素油 苯扎xiu铵溶液 苯甲酸 苯甲酸钠 枸橼酸 枸橼酸钠 枸橼酸钾 盐酸苯海拉明 盐酸丁卡因 盐酸普鲁卡因 葡萄糖酸锌 无水硫酸镁 七水硫酸镁 倍他米松 曲安奈德 淀粉糊精 羧甲基纤维素钠 吡拉西坦 碘酊 碘伏 单双硬脂酸甘油酯 安乃近 葡萄糖糖 壳聚糖 二甲基硅油粘度 二甲基亚砜 聚乙二醇各型号 聚乙烯醇 卡波姆940 盐酸林可霉素 克林霉素 利凡诺 轻质液状石蜡 橙皮酊 山梨酸钾 聚山梨酯吐温80等千余种医药用级的原辅料,资质齐全欢迎来电订购 比旋度 取本品,精密称定,加无水乙醇溶解并定量稀释制成每1ml中约含40mg的溶液,依法测定(通则0621),比旋度为+102.5°至+107.5°(应于容器开启后30分钟内取样,并在溶液配制后30分钟内测定)。 吸收系数 取本品,精密称定,加无水乙醇溶解并定量稀释制成每1ml中约含10μg的溶液,照紫外-可见分光光度法(通则0401),在265nm的波长处测定吸光度,吸收系数()为460~490。 【鉴别】 (1)取本品约0.5mg,加三氯甲烷5ml溶解后,加醋酐0.3ml与硫酸0.1ml,振摇,初显黄色,渐变红色,迅即变为紫色,最后成绿色。 (2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。 (3)本品的红外光吸收图谱应与对照的图谱(光谱集452图)一致。 【检查】 麦角甾醇 取本品10mg,加90%乙醇2ml溶解后,加洋地黄皂苷溶液(取洋地黄皂苷20mg,加90%乙醇2ml,加热溶解制成)2ml,混合,放置18小时,不得发生浑浊或沉淀。 有关物质 照高效液相色谱法(通则0512)测定。 供试品溶液 取本品约25mg,置100ml棕色量瓶中,加异辛烷80ml,避免加热,超声使完全溶解,放冷,用异辛烷稀释至刻度,摇匀。 对照溶液 精密量取供试品溶液1ml,置100ml棕色量瓶中,用异辛烷稀释至刻度,摇匀。 色谱条件 见含量测定项下。进样体积100μl。 系统适用性溶液与系统适用性要求 见含量测定项下。 测定法 精密量取供试品溶液与对照溶液,分别注入液相色谱仪,记录色谱图至维生素D2峰保留时间的2倍。 限度 供试品溶液色谱图中如有杂质峰,除前维生素D2峰外,单个杂质峰面积不得大于对照溶液主峰面积的0.5倍(0.5%),各杂质峰面积的和不得大于对照溶液主峰面积(1.0%)。 【含量测定】 取本品,照维生素D测定法(通则0722第一法)测定,即得。 【类别】 维生素类药。 【贮藏】 遮光、充氮、密封,在冷处保存。

乳酸依沙吖啶(Lactose Ipecacuanha)是一种药用级的原料药物,符合CP2020(中国药典2020版)的药典标准。它主要用于制备医药产品,具有多种医疗应用。
乳酸依沙吖啶是由乳糖和依沙吖啶组成的复合物。乳糖是一种天然的二糖,具有良好的溶解性和稳定性,可以作为药物的辅助材料,用于提高药物的稳定性和流动性。依沙吖啶则是一种中枢神经系统的解毒剂,能够中和体内的毒素,减轻中毒症状,并促进体内毒素的排出。

作为医药级原料,乳酸依沙吖啶需要符合CP2020的标准。根据CP2020,乳酸依沙吖啶的质量要求包括外观、含量、溶解度、重金属、微生物限度等多个方面。外观要求为白色或几乎白色结晶或结晶性粉末,无异味;含量要求为乳糖与依沙吖啶之和的质量百分比在 88.0%~94.0%之间;溶解度要求在无痕迹地溶解于水中;重金属的限定值要符合规定的安全标准;微生物限度要符合规定的标准。
乳酸依沙吖啶的生产需要严格按照CP2020的规定进行,包括原料采购、生产工艺、质量控制等方面。生产过程中需要进行多项质量控制,包括原料质量检验、过程监控和最终产品的质量检验。这样可以确保乳酸依沙吖啶的质量符合CP2020的要求,保证其在医药产品中的安全性和有效性。
乳酸依沙吖啶作为一种重要的药用级原料药物,具有广泛的应用前景。它可以用于制备各种医药产品,比如止咳药、解毒剂等。其优良的物理化学性质和质量标准保证了医药产品的质量和疗效。同时,乳酸依沙吖啶的生产也需要遵守相关法规和规范,确保药物的安全和有效性。
总之,乳酸依沙吖啶作为一种药用级原料,符合CP2020的药典标准,具有广泛的医疗应用前景。通过在生产过程中严格控制质量,可以保证乳酸依沙吖啶的质量符合要求,并能在医药产品中发挥良好的作用。

酮康唑
Tongkangzuo
Ketoconazole
C26H28Cl2N4O4531.44
【性状】本品为类白色结晶性粉末;无臭。
本品在中易溶,在甲醇中溶解,在乙醇中微溶,在水中几乎不溶。
熔点本品的熔点(通则0612)为147~151℃。
【鉴别】(1)取本品约10mg,加0.1mol/L盐酸溶液5ml,使溶解,加碘化铋钾试液数滴,即生成橙红色沉淀。
(2)取本品约60mg,置100ml量瓶中,加0.1mol/L盐酸溶液10ml溶解,用水稀释至刻度,摇匀,取适量,用0.01mol/L盐酸溶液稀释制成每1ml中含15μg的溶液,照紫外-可见分光光度法(通则0401)测定,在221nm与269nm的波长处有最大吸收,在276nm的波长处有一肩峰。
(3)本品的红外光吸收图谱应与对照的图谱(光谱集677图)一致。
【检查】旋光度取本品,精密称定,加二氯甲烷溶解并定量稀释制成每1ml中约含100mg的溶液,依法测定(通则0621),旋光度应为一0.1°至+0.l°。

苄达赖氨酸原料药生产厂家,苄达赖氨酸药用辅料批发价格,苄达赖氨酸医药级,苄达赖氨酸药用级,苄达赖氨酸国药准字号原料,cp2020标准苄达赖氨酸
本品为L-赖氨酸(1-苄基-1H-吲哒唑-3-氧基)乙酸盐。按干燥品计算,含C6H14N2O2•C16H14N2O3不得少于98.5%。
【性状】 本品为白色或类白色的结晶性粉末;无臭。

本品在水中溶解,在乙醇和三氯甲烷中几乎不溶。
熔点 本品的熔点(通则 0612)为179~184℃。
吸收系数 取本品,精密称定,加水溶解并定量稀释制成每1ml中约含40µg的溶液,照紫外-可见分光光度法(通则 0401),在307nm的波长处测定吸光度,吸收系数(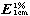 )为125~135。
)为125~135。
【鉴别】(1)取本品,加水溶解并稀释制成每1ml中含30µg的溶液,照紫外-可见分光光度法(通则 0401)测定,在307nm的波长处有最大吸收,在272nm的波长处有最小吸收。
(2)本品的红外光吸收图谱应与对照的图谱(光谱集 1284图)一致。
【检查】酸碱度取本品1.0g,加水50ml溶解后,依法测定(通则 0631),pH值应为5.5~7.5。
溶液的澄清度与颜色 取本品0.1g,加水10ml溶解后,溶液应澄清无色;如显色,与黄色1号标准比色液(通则 0901第一法)比较,不得更深。
有关物质 取本品,加水溶解并稀释制成每1ml中约含1mg的溶液,作为供试品溶液;精密量取1ml,置100ml量瓶中,用水稀释至刻度,摇匀,作为对照溶液。 照高效液相色谱法(通则 0512)测定,用十八烷基硅烷键合硅胶为填充剂;以乙腈-0.1mol/L醋酸溶液(47:53)为流动相;检测波长为307nm。理论板数按苄达赖氨酸峰计算不低于3000,苄达赖氨酸峰与各杂质峰的分离度应符合要求。精密量取供试品溶液与对照溶液各20µl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的5倍。供试品溶液的色谱图中如有杂质峰,各杂质峰面积的和不得大于对照溶液的主峰面积(1.0%)。
干燥失重 取本品,在105℃干燥至恒重,减失重量不得过1.0%(通则 0831)。
炽灼残渣 取本品1.0g,依法检查(通则 0841),遗留残渣不得过0.2%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则 0821第二法),含重金属不得过百万分之二十。
【含量测定】取本品0.2g,精密称定,加冰醋酸20ml溶解后,加结晶紫指示液1滴,用高氯酸滴定液(0.1mol/L)滴定至溶液显蓝绿色,并将滴定的结果用空白试验校正。每1ml的高氯酸滴定液(0.1mol/L)相当于21.42mg的C6H14N2O2•C16H14N2O3。
【类别】眼科用药。
【贮藏】密封,在干燥处保存。

医药级液状甘油磷酸钠原料有资质批文
医药级液状甘油磷酸钠原料有资质批文
甘油磷酸钠为营养药,是静脉磷补充剂,用于满足人体每天对磷的需要。磷可参与骨质的形成,以磷脂形式参与细胞膜组成,同时与多种代谢中的酶活性有关,在能量代谢中作用至关重要。
甘油磷酸钠主要的作用为成人静脉营养的磷补充剂,还可适用于磷缺乏的患者,需要注意的是长期用药可引起血磷、血钙浓度的变化。
适应症
本品为中枢神经营养剂,主要用于神经衰弱。
用量用法
用于配制复方甘油磷酸盐制剂。
储存、有效期
[制剂] 溶液剂:50%。

维生素B9原料药生产厂家,维生素B9药用辅料批发价格,维生素B9医药级,维生素B9药用级,维生素B9国药准字号原料,cp2020标准维生素B9
维生素B9,也称为叶酸,是人体所需的一种维生素。它是一种水溶性维生素,能够参与人体的许多代谢过程。维生素B9对于孕妇和儿童的生长发育尤为重要,因为它能够促进胎儿脑部和神经系统的正常发育,防止唇腭裂、脊柱裂等先天畸形的发生。

维生素B9在人体内的主要作用是参与细胞分裂和DNA的合成。维生素B9的缺乏会导致DNA合成减少,影响细胞的正常分裂和生长,使得红细胞生成减少,引起巨幼红细胞性贫血。此外,维生素B9缺乏还会影响神经系统的正常发育和功能,导致失眠、头晕、乏力、记忆力减退、神经衰弱等症状。
日常饮食中,富含维生素B9的食物包括动物肝脏、蛋黄、牛奶、豆类、酵母、绿叶蔬菜等。此外,为了预防维生素B9的缺乏,许多国家在面粉中添加叶酸,以保证人们正常的需求量。
值得注意的是,维生素B9也有一定的安全性问题。在服用大剂量的叶酸补剂时,可能会增加癌症和心血管疾病的风险。因此,建议在医生的指导下合理地补充叶酸。特别是孕妇,应该在医生的指导下补充叶酸,以保证胎儿的正常发育。
综上所述,维生素B9作为一种重要的维生素,对于人体的正常生长发育和代谢过程有着重要的作用。在日常饮食中,适量地摄入富含叶酸的食物,可以保证人体的正常需求量。在补充叶酸时,应该遵循医生的指导,以避免安全性问题的发生。