 该商家已通过实名认证
该商家已通过实名认证
产品名称:他克莫司
英文名:Tacrolimus
剂型规格:注射液:1ml:5mg胶囊:0.5mg、1mg、5mg缓释胶囊:0.5mg、1mg、5mg软膏:0.03%(10g:3mg)、0.1%(10g:10mg)滴眼液:0.1%(5ml:5mg)
适应症:1.注射液用于预防肝脏或肾脏移植术后的移植物排斥反应。治疗肝脏或肾脏移植术后应用其他免疫抑制药物无法控制的移植物排斥反应。2.软膏适用于因潜在危险而不宜使用传统疗法、或对传统疗法反应不充分、或无法耐受传统疗法的中到重度特应性皮炎患者,作为短期或间歇性长期治疗。3.滴眼液适用于抗过敏治疗效果不明显的春季角结膜炎患者。应在观察到眼睑结膜巨大乳头增殖时使用。
科室:皮肤科,肝肾移植科
家数:进口制剂4家,国产制剂12家;原料4进7国;
产品优势:他克莫司作为一种强力的新型免疫抑制剂,主要通过抑制白介素-2(L-2)的释放,全面抑制T淋巴细胞的作用,较环孢素(CsA)强100倍。他克莫司作为肝、肾移植的一线用药,已在日本、美国等14个国家上市。临床实验表明,其在心、肺、肠、骨髓等移植中应用有很好的疗效。同时他克莫司在治疗特应性皮炎(AD)、系统性红斑狼疮(SLE)、自身免疫性眼病等自身免疫性疾病中也发挥着积极的作用。
原料来源:印度
备案状态:I
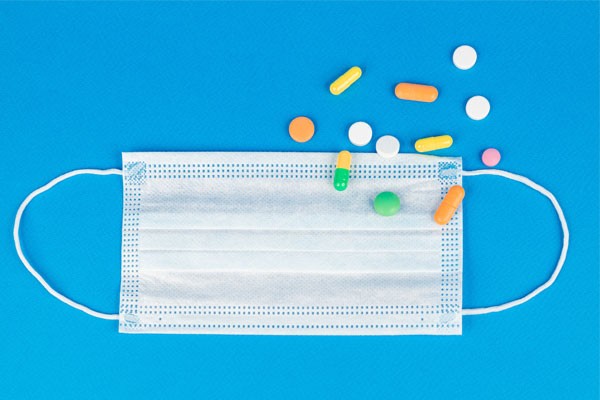




[3S-[3R[E(1S,3S,4S)],4S,5R,8S,9E,12R,14R,15S,16R,
18S,19S,26aR]]-5,6,8,11,12,13,14,15,16,17,18,19,24,25,26,26a-十六氢-5, 19-二羟基-3-[2-(4-羟基-3-甲氧基环已基)-1-甲基乙烯基]-14, 16-二甲氧基-4,10,12,18-四甲基-8-(2-丙烯基)-15,19-环氧-3H-吡啶并[2,1-c][1,4]氧杂氮杂环二十三碳烷-1,7,20,21(4H,23H)-四酮一水合物
在分子水平,他克莫司的作用显然是利用与细胞性蛋白质(FKBP12)相结合,而在细胞内蓄积产生效用。FKBP12-他克莫司复合物会专一性地结合以及抑制calcinurin,其会抑制T细胞中所产生钙离子依赖型讯息传导路径作用,因此防止不连续性淋巴因子基因的转录。本药是具有高度免疫抑制的药物,其活性在体外及体内实验中都已被证实。本药抑制形成主要移植排斥作用之细胞毒性淋巴球的生成。本药抑制T细胞的活化作用以及T辅助细胞依赖B细胞的增生作用。也会抑制如白介素-2、白介素-3及γ-干扰素等淋巴因子的生成与白介素-2受体的表达。在分子水平,本药的效应似乎是由结合到细胞性蛋白质(FKBP)所产生,此蛋白质也会造成该化合物累积在细胞间。在体内试验中发现,本药显示出对肝脏及肾脏移植有效。
肝脏.心脏.肾脏及骨髓移植患者的首选免疫抑制药物,移植后排斥反应对传统免疫抑制方案耐药者,也可选用该药物。不良反应与环孢霉素相似。
下列口服及静脉注射给药之建议剂量只是概略指标,本药的实际剂量应依据个别病人的需要而加以调整,建议剂量只有起始剂量,因此治疗过程中应藉由临床判断并辅以他克莫司血中浓度的监测以调整剂量。口服给药每日剂量分两次投予。最好是在空腹或至少进食前1hr或进食后2-3hr服用胶囊,以达到最大吸收量。口服胶囊时,通常须连续服用以抑制移植排斥作用。并没有治疗期间的限制。静脉注射给药输注用浓缩液必须在聚乙烯或玻璃瓶中用5%葡萄糖注射或者生理食盐水稀释。所形成的最终输注用溶液的浓度必须在0.004-0.1mg/ml范围间。24hr内输注20-250ml。此溶液不可以一次全量快速注释给药。当患者的状况允许时,应尽快将静脉注射疗法改为口服疗法。静脉注射疗法不应该连续超过7天。首次免疫抑制剂量 - 成人肝脏移植者为0.1-0.2mg/kg/天,肾脏移植患者为0.15-0.3mg/kg/天,分2次口服。应该在肝脏移植手术后约6hr以及肾脏移植手术24hr内开始给药。如果病患的临床状况不适于口服给药,则应该给予连续24hr的静脉输注他克莫司治疗。起始静脉注射剂量对肝脏移植患者为0.01-0.05mg/kg/天,而对肾脏移植患者为0.05-0.1mg/kg/天。首次免疫抑制剂量 - 儿童儿童病患通常需要成人建议剂量的1.5-2倍,才能达到相同的治疗血浓度。肝脏及肾脏移植:0.3mg/kg/天,分2次口服。如果不能口服给药时,应该给予连续24hr的静脉输注,对肝脏移植的儿童为0.05mg/kg/天,而对肾脏移植的儿童为0.1mg/kg/天。维持治疗需要口服本药来达到连续免疫抑制作用以维持移植物的生存。在维持治疗中常可减低剂量。主要是根据各病患个体对于排斥及耐受性的临床评估而调整。在病患手术后的恢复期,本药的药物动力学可能会改变,因此需要调整本药的剂量。如果疾病发生变化(例如产生排斥现象),必须考虑更换免疫抑制疗法。增加激素、使用短期的单株/多株抗体以及增加本药的剂量都曾被用来控制排斥发作。如果有中毒征兆(例如明显的不良反应)出现,必须降低本药的剂量。当本药和激素合用时,激素用量通常可以减低,且在少数病例中可以持续地进行单一治疗法。对传统免疫抑制治疗无效如果病患以传本药的治疗应该以该特定移植中首次免疫抑制所建议的初始剂量来开始给药。同时给予环孢素及本药可能会延长环孢素的半衰期,并且产生毒性作用。应该在考虑环孢素的血浓度以及病患的临床状况后,方可开始使用本药治疗。实际上,通常是在停止给予环孢素后12-24hr才开始使用本药。由于环孢素后的清除率可能会受影响,所以在换药后应该监测环孢素的血药浓度。特殊病人肝功能不全之病患;对于手术前或手术后功能不全,如最初移植功能不良的病患可能需要减低剂量。肾功能不全之病患:由于他克莫司的肾清除率很低,所以依据药物动力学的原则是不需要调整剂量。但是由于其潜在肾毒性,所以建议小心监测包括血肌酐、肌酐清除率的计算及排尿量等肾功能。本药的血中浓度不因透析而降低。老年病患有限的经验显示其剂量应同成年患者。
由于大部分用药者存在有严重的疾病和同时并用许多其它药物,常很难确定与免疫抑制药物有关之不良反应。有证据显示,下列许多药物不良反应是可逆转的,并且可经由剂量降低而改善。和静脉给药相比,口服给药发生不良反应的频率明显地较低。下列药物不良反应乃是依据身体系统及其发生频率来编排的。心血管系统 - 经常性:高血压。偶发生:心绞痛、心悸、渗液(例如心包积液、胸膜积液)。罕见性:包含休克之低血压、心电图异常、心律失常、心房/心室纤颤以及心跳停止、血栓静脉炎、出血(例如胃肠道、大脑)、心力衰竭、心脏扩大、心跳缓慢.
胶囊1mg*10粒,50粒,5mg*5粒,50粒。注射液5mg/1ml*10安瓿。

桐晖药业 -提供原料药、参比制剂、杂质对照品、进口药品注册代理、致力于为客户提供一站式整体解决方案,欢迎来电咨询!
中文名称:罗红霉素EP杂质H
英文名:Roxithromycin EP Impurity H
CAS号:425365-65-7
产品编码:REF-R05009
分子式:C41H76N2O14
分子量:821.06
纯度:98.86%
产品性质:客户定制
外观性状:白色固体
储存条件:-20℃
化学名称:(3R,4S,5S,6R,7R,9R,11S,12R,13R,14R,E)-6-(((2S,3R,4S,6R)-4-(dimethylamino)-3-hydroxy-6-methyltetrahydro-2H-pyran-2-yl)oxy)-14-ethyl-7,12-dihydroxy-4-(((2R,4R,5S,6S)-5-hydroxy-4-methoxy-4,6-dimethyltetrahydro-2H-pyran-2-yl)oxy)-10-(((2-methoxyethoxy)methoxy)imino)-3,5,7,9,11,13-hexamethyloxacyclotetradecan-2-one
罗红霉素EP杂质H,罗红霉素EP杂质H标准品,罗红霉素EP杂质H对照品

产品名称:盐酸美克洛嗪
英文名:Meclizine hydrochloride
剂型规格:片剂 12.5 mg;25mg; 50mg
适应症:适用于治疗与影响前庭系统的疾病有关的眩晕。前庭系统的疾病有关的眩晕。
科室:耳鼻喉科
家数:国1A+0
产品优势:印度外商USDMF,可给总代
原料来源:印度外商
备案状态:未备案


中文别名: 美克洛嗪、氯苯甲嗪、氯苯苄嗪、美可利嗪、美可洛秦、美可洛嗪、美克利嗪、美其敏、敏可静、敏克静、盐酸氯苯甲嗪、盐酸氯苯苄嗪、盐酸美克洛嗪
英文别名: Ancolan、Antivert、Bonamina、Bonamine、Bonine、Calmonal、Diadril、Histametizine、Itimerol、Marex、Meclizine、Meclizine Hydrochloride、Meelizine
分子式: C25H27ClN2
分子量:390.95
CAS No :569-65-3
药品类别: 抗组织胺药
药理药动:是组胺受体的拮抗剂,其作用远较苯海拉明持久,可维持 12—24小时。
本品为淡黄色至黄色结晶性粉末;微臭,无味。在三氯甲烷中易溶,在乙醇中溶解,在水中极微溶解,在乙醚中几乎不溶。
沸点230℃(0.267kPa)
其盐酸盐([1104-22-9])
熔点224℃(分解)
适用于各种皮肤粘膜过敏疾病,亦可用于妊娠、放疗及晕动症引起的恶心、呕吐。是组胺受体的拮抗剂,其作用远较苯海拉明持久,可维持12~24小时。
[制剂与规格]盐酸美克洛嗪pian25mg
不良反应
有嗜睡、视力模糊、乏力等反应
本品为组胺受体的拮抗剂,可对抗组胺引起的降压效应、并对致死量组胺引起的动物死亡起保护作用。并有中枢抑制和局麻作用。抗晕动症和眩晕效应与其抗胆碱作用有关。皮肤粘膜过敏性疾病,亦可用于放疗及晕动症引起的恶心、呕吐。
口服,25mg/次,3次/日。预防晕动病应提前1小时服药,每次25 ~ 50mg,每日1次。
[药物过量] 过量可能引起精神错乱、抽搐、震颤、呼吸困难、低血压。如服用中毒量,可用生理盐水洗胃和导泻。抽搐时可静注地西泮控制。低血压者可使用血管收缩药对症治疗,其他包括给氧和静脉输液等支持疗法。
妊娠B类。对本品过敏者禁用。
(1)在下列情况下应慎用膀胱颈狭窄、良性前列腺肥大、闭角型青光眼、幽门十二指肠狭窄等。
(2)本品可抑制组胺引起的皮肤反应,在药物过敏性皮试前72小时应停用本品,以免出现假阴性反应结果。
[孕妇及哺乳期妇女用药]大鼠超过人常用剂量25~50倍可见幼仔腭裂。经药物流行病调查,未发现不良反应。医生应用于孕妇时应权衡利弊。因本品可进入乳汁,哺乳期妇女不宜用。
[儿童用药] 新生儿、早产儿不宜用。
[老年患者用药]老年人对成人常规剂量较敏感,易发生低血压、精神错乱、滞呆和头晕,应酌情减量。

产品名称:曲前列尼尔
英文名:Treprostinil
剂型规格:注射液,20ml:20mg20ml:50mg20ml:100mg20ml:200mg
适应症:治疗致命性孤儿疾病的药物:肺动脉高压(PAH)
科室:心血管内科
家数:制剂:1进口
产品优势:2013年4月在中国获批进口制剂批文,是目前用于治疗PAH国内唯一皮下/静脉给药的前列环素类药物。曲前列尼尔可扩张(加宽)动脉,减少体内凝血血小板的数量,从而降低了从心脏到肺部的肺动脉血压。临床试验表明,曲前列尼尔治疗先天性心脏病并重度PAH可改善肺部氧合情况,而对体循环压力无明显影响,对于缩短气管插管时间、减少重症监护室停留时间、加速患儿的康复具有重要意义。
原料来源:印度
备案状态:未备案



本品主要成份为曲前列尼尔。
化学名称:[[(1R, 2R, 3aS, 9aS)-2, 3, 3a, 4, 9, 9a-六氢-2-羟基-1-[(3S)-3-羟基辛烷基]-1 H -苯并[f]茚-5-基]氧基]乙酸
化学结构式:
https://x1.webres.medlive.cn/drugref/ChemPreparationDetail/201411251019180789.jpg" style="border-radius: 10px;display: block;margin: 20px auto;max-width: 95%;">
本品为无色至微黄色的澄明液体。
本品用于治疗肺动脉高压(PAH, WHO分类1)﹐以减轻运动引起的相关症状。在建立本品疗效的研究中﹐研究受试者包括NYHA功能分级II~IV级的原发性和遗传性肺动脉高压(58%)﹑与先天性体肺循环分流相关的肺动脉高压(23%)以及与结缔组织疾病相关的肺动脉高压(19%)。
(1)20ml : 20mg (2)20ml : 50mg (3)20ml : 100mg (4)20ml : 200mg
本品用20ml玻璃瓶包装﹐共有四个规格﹐分别含有20﹑50﹑100或200mg曲前列尼尔(1mg/ml﹑2.5mg/ml﹑5mg/ml或10mg/ml)。本品输注前需用注射用水或0.9%NaCl注射液稀释。本品的给药方式为皮下或静脉注射给药。
本品只能连续皮下(SC)或静脉(IV)输注。皮下输注是首选给药路径﹐但是﹐如果因为输注部位严重疼痛或反应而不能耐受皮下给药﹐也可经中心静脉导管给药。初始输注速率为1.25ng/kg/min。如果由于全身效应不能耐受初始剂量﹐应将注射速率降低至0.625ng/kg/min。
剂量调整
长期剂量调整的目标是确定曲前列尼尔的剂量﹐使其可改善肺动脉高压症状﹐同时减少本品的其他药理学效应(头痛﹑恶心﹑呕吐﹑坐立不安﹑焦虑以及输注部位疼痛或反应)。
根据临床疗效进行剂量调整。在治疗的前四周﹐输注速率的增加值为每周1.25ng/kg/min﹐之后为每周2.5ng/kg/min。如能够耐受﹐可以更高频率调整剂量。剂量>40ng/kg/min的临床应用经验非常少。应避免突然停止输注。可在中断数小时
内重新以相同剂量速率给药﹐如果中断时间较长可能需要重新滴定剂量。
对于轻至中度肝功能不全患者﹐本品初始剂量应为0.625ng/kg/min﹐给药剂量应按理想体重计算﹐剂量增加须谨慎。尚未在严重肝功能不全患者中进行研究。
肾功能不全患者
尚未对肾功能不全患者进行研究。
用药方法:
注射给药前﹐应目检药品中是否存在颗粒物和变色。如本品存在颗粒物或变色﹐则不可使用。
<皮下输注>
本品使用皮下药物专用的输液泵﹐经插入式皮下导管连续皮下输注给药。为避免药物输注中断﹐在发生此情况时患者必须可立即获得备用输液泵和皮下输液器具。
本品给药使用的移动式输液泵应满足以下要求:(1)体积小﹑重量轻;(2)最低输注速度可调整限度约为0.002ml/h;(3)在输液管阻塞/不输液﹑设备电量低﹑程序错误和马达故障时﹐应有报警提醒;(4)输液速度准确率在±6%或更佳;(5)正压驱动。贮液器应由聚氯乙烯﹑聚丙烯或玻璃制成。
根据患者剂量(ng/kg/min)﹑体重(kg)以及药品规格(mg/ml)计算皮下输注速率(ml/h)﹐无需进一步稀释。使用过程中﹐装有未稀释本品的贮液器(注射器)在37℃条件下可给药至72h。用下列公式计算皮下输注速率:
https://x1.webres.medlive.cn/drugref/ChemPreparationDetail/201411251038130501.jpg" style="border-radius: 10px;display: block;margin: 20px auto;max-width: 95%;">
无。
药物输送系统导致的风险
本品采用留置中心静脉导管长期静脉输注。这种给药途径可导致血流感染(BSIs)和败血症﹐可能是致命的。因此﹐连续皮下输注(未稀释)是首选给药方式。
一项曲前列尼尔静脉给药开放试验中(n=47)﹐在大约35患者年中有7例导管相关感染﹐或每使用5年约有1例次BSI事件。疾控中心在7家研究中心的调查发现﹐静脉注射曲前列尼尔治疗PAH﹐每用药3年约发生1次BSI(血液细菌培养阳性)。
一般使用条件
只有具有诊断和治疗肺动脉高压经验的临床医生可以使用本品。
本品是一种强效的肺部和全身血管扩张剂。本品必须在具有足够的生理监控和紧急救护人员及设备的医疗场所开始给药。本品可长期使用﹐但应慎重考虑患者使用本品和维护注射系统的能力。
剂量调整
如症状未改善或恶化应增加剂量﹐如出现过度药理效应或不可接受的输注部位症状应减少剂量。
突然停药或突然大幅降低剂量
突然停药或突然大幅降低剂量可能会导致肺动脉高压症状恶化﹐应避免突然停药或突然大幅降低剂量。
肝或肾功能不全患者
肝或肾功能不全患者应缓慢增加剂量﹐因为与肝﹑肾功能正常患者相比﹐这些患者全身暴露浓度可能更大。
其它药物对曲前列尼尔的作用
同时服用细胞色素P450(CYP)2C8酶抑制剂(如吉非贝齐)可增加曲前列尼尔暴露量(C max 和AUC)。同时服用CYP2C8酶诱导剂(如利福平)可降低曲前列尼尔暴露量。暴露量升高可能会增加与曲前列尼尔有关的不良事件﹐而暴露量减少可能降低临床疗效。
1﹑孕妇用药:
妊娠大鼠﹐在器官形成和妊娠后期以高达900ng/kg/min速率(约为人初始输注速率的117倍﹐以ng/m 2 计﹐约为临床试验达到的平均速率的16倍)连续皮下输注曲前列尼尔﹐未对胎仔造成伤害。妊娠家兔﹐在胎仔器官形成期以150ng/
kg/min速率(约为人初始输注速率的41倍﹐以ng/m 2 计﹐约为临床试验使用的平均速率的5倍)连续皮下输注曲前列尼尔﹐使胎仔骨骼变异(两侧肋骨或腰上右雏肋)的发生率以及母体毒性(体重和食量下降)增加。大鼠从妊娠至哺乳结束
以最高450ng/kg/min速率连续皮下输注曲前列尼尔﹐对幼仔的生长和发育无影响。
由于动物生殖试验不一定能预示人体反应﹐所以妊娠期间应慎用本品。
动物试验未观察到曲前列尼尔对生产和分娩有治疗相关影响。曲前列尼尔对人类生产和分娩的影响尚不清楚。
2﹑哺乳期妇女用药 。
尚不清楚曲前列尼尔是否通过人乳汁分泌或口服后被全身吸收。鉴于多种药物均经人乳汁排泄﹐所以哺乳期妇女应慎用本品。
尚未确定本品在儿童患者中的安全性和有效性。临床试验中年龄≤16岁患者数量较少﹐故不能确定儿童患者的反应是否与成年患者不同。总之﹐必须谨慎选择剂量。
临床试验未包括足够数量年龄≥65岁的患者﹐故不能确定老年患者的反应是否不
同于年轻患者。总之﹐考虑到老年患者的肝﹑肾或心脏功能衰退﹐以及伴随疾病或应用其他药物治疗的比率更高﹐老年患者的剂量选择应特别慎重。
目前已经研究了曲前列尼尔皮下给药(本品)和口服给药(曲前列尼尔二乙醇胺)的药物代谢动力学/药效学相互作用。
药效学相互作用:
◆ 抗高血压药物或其它血管扩张剂
本品与利尿剂﹑抗高血压药物或其它血管扩张剂合用﹐可能增加症状性低血压的风险。
◆ 抗凝血剂
由于曲前列尼尔抑制血小板聚集﹐所以可能会增加出血风险﹐尤其是正在服用抗凝血剂的患者。
药代动力学相互作用:
◆ 波生坦
在用波生坦(250mg/天)和曲前列尼尔口服剂(曲前列尼尔二乙醇胺)进行的一项人体药物代谢动力学研究中,未观察到两者之间有相互作用。
◆ 西地那非
在用西地那非(60mg/天)和曲前列尼尔口服剂(曲前列尼尔二乙醇胺)进行的一项人体药物代谢动力学研究中﹐未观察到两者之间有相互作用。
◆ 曲前列尼尔对细胞色素P450酶的作用
人肝微粒体的体外试验显示﹐曲前列尼尔既不抑制细胞色素P450(CYP)同工酶CYP1A2﹑CYP2A6﹑CYP2C8﹑CYP2C9﹑CYP2C19﹑CYP2D6﹑CYP2E1和CYP3A﹐也不诱导细胞色素P450同工酶CYP1A2﹑CYP2B6﹑CYP2C9﹑CYP2C19和CYP3A。因此﹐ 对于经CYP酶代谢的化合物﹐本品对其药物代谢动力学没有影响。
◆ 细胞色素P450抑制剂和诱导剂对曲前列尼尔的作用
曲前列尼尔口服剂(曲前列尼尔二乙醇胺)的人体药物代谢动力学研究表明﹐合用细胞色素P450(CYP)2C8酶抑制剂吉非贝齐可使曲前列尼尔的暴露量(C max和AUC)增加。与CYP2C8酶诱导剂利福平联合给药则降低曲前列尼尔的暴露量(C max 和AUC)。尚未测定CYP2C8抑制剂或诱导剂是否会改变曲前列尼尔非肠道
给药(皮下或静脉)的安全性和疗效。
◆ 其它药物对曲前列尼尔的作用
健康志愿者口服或皮下注射曲前列尼尔﹐同时分别以扑热息痛(4g/天)﹑华法林(25mg/天)和氟康唑(200mg/天)给药﹐研究药物相互作用。这些研究显示﹐对曲前列尼尔药代动力学的影响没有临床意义。曲前列尼尔不影响华法林的药代动力学或药效动力学。对接受单剂量25mg华法林给药的健康受试者﹐以10ng/kg/min注射速率连续皮下输注曲前列尼尔﹐对R-和S-华法林的药代动力学以及国际标准化比值(INR)没有影响。
在临床试验期间﹐本品用药过量的体征和症状是剂量限制性药理学效应的扩大﹐包括潮红﹑头痛﹑低血压﹑恶心﹑呕吐以及腹泻。大部分事件是自限性的﹐在降低剂量或停止用药后消失。
在对照临床研究中有7例患者接受了超剂量给药﹐在随后的开放治疗中又有7例患者接受了超剂量给药;这些超剂量事件是由于意外注射给药﹑输液泵给药速率程序错误以及处方剂量错误所致。有2例患者因本品输送过量产生了重大的血液动力学相关不良反应(低血压﹑近乎晕厥)。
1名儿童患者经中心静脉导管意外给予曲前列尼尔7.5mg﹐出现的症状包括潮红﹑头痛﹑呕吐﹑低血压和癫痫并出现几分钟的意识丧失。随后﹐该患者的上述症状消失。
PAH 临床试验
在两个12周﹑多中心﹑随机双盲试验中﹐比较了470名NYHA II级(11%)﹑III级(81%)或IV级(7%)PAH患者连续皮下输注本品和安慰剂的疗效。58%患者的肺动脉高压为原发性/遗传性肺动脉高压﹐19%患者为结缔组织疾病相关肺动脉高压﹐23%患者为先天性体肺分流相关肺动脉高压。这些患者的平均年龄为45岁(9~75岁)。约81%的患者为女性﹐84%的患者为白种人。肺动脉高压平均病龄为3.8年。该项研究的主要终点为患者6分钟步行距离的变化﹐此为一种测定运动耐量的标准方法。研究中还对众多心力衰竭相关的症状进行评价﹐但是本品给药引发的局部不适和疼痛实际上已经使这些评估揭盲。由不参与研究中其他项目的人员负责对6min步行距离﹑步行过程中气短的主观测定(Borg呼吸困难评分)进行评价。曲前列尼尔注射液皮下注射给药﹐第12周时﹐曲前列尼尔的平均剂量为9.3ng/kg/min﹐极少数受试者的治疗剂量>40ng/kg/min。患者的基础治疗由研究者决定﹐包括抗凝血剂﹑口服血管扩张剂﹑利尿剂﹑地高辛和氧气﹐但不包括内皮素受体拮抗剂或依前列醇。此两项研究的设计完全一致并同步进行﹐对其研究结果进行汇总分析和单独分析。
血液动力学效应
如表3所示﹐本品长期治疗导致血液动力学的轻微变化﹐这与肺和全身血管舒张有关。
https://x1.webres.medlive.cn/drugref/ChemPreparationDetail/201411251137070299.jpg" style="border-radius: 10px;display: block;margin: 20px auto;max-width: 95%;">
药理作用
曲前列尼尔主要通过直接舒张肺和全身动脉血管床并抑制血小板聚集发挥作用。动物试验可见其血管扩张效应﹐减少右心室和左心室后负荷﹐增加心输出量和心搏出量。试验显示曲前列尼尔可引起剂量相关的负性肌力和舒张效应。尚未观察到对心脏传导存在明显影响。
曲前列尼尔可导致血管舒张和心动过速。单次吸入曲前列尼尔84μg对QTc的影响不大且持续时间短﹐但可能是心率快速变化的一种假象。曲前列尼尔皮下或静脉给药的药物浓度比吸入途径暴露的浓度高很多倍;曲前列尼尔经非肠道给药对QTc间期的影响尚未知。
毒理研究
遗传毒性:
曲前列尼尔Ames试验﹑TK+/-小鼠淋巴瘤正向突变试验﹑大鼠微核试验结果均为阴性。
生殖毒性:
雄性大鼠从交配前10周开始至2周交配期连续给药﹐雌性大鼠从交配前2周开始至妊娠第6天连续给药﹐皮下输注曲前列尼尔450ng/kg/min(以ng/m计﹐约为人体推荐初始输注速率1.25ng/kg/min的59倍)﹐为临床试验平均给药速率9.3ng/kg/min的8倍)﹐未见对雌﹑雄动物生育力或交配行为的明显影响。妊娠大鼠在子代器官形成期和妊娠后期连续皮下输注曲前列尼尔速率达900ng/kg/min(以ng/m计﹐约为人初始输注速率的117倍﹐约为临床试验平均给药速率的16倍)﹐未见对胚胎-胎仔生长发育的明显影响。妊娠兔在子代器官形成期连续皮下输注曲前列尼尔速率达150ng/kg/min(以ng/m计﹐约为人初始输注速率的41倍﹐约为临床试验平均给药速率的5倍)﹐可见胎仔骨骼变异发生率(两侧肋骨或第1腰椎右侧退化肋骨)增加﹐以及母体毒性(体重和摄食量下降)。
大鼠围产期皮下输注曲前列尼尔最高速率达450ng/kg/min﹐未见对幼仔生长发育的明显影响。
在1.25~125ng/kg/min范围内﹐曲前列尼尔注射液连续皮下给药的药代动力学呈线性(对应的血浆浓度约为15~18250pg/ml)﹐可用二室模型描述。尚未研究输注速率大于125ng/kg/min的剂量比例关系。
以10ng/kg/min的剂量给药达稳态时﹐本品皮下和静脉注射给药具有生物等效性。
吸收
在皮下注射后﹐本品被迅速和完全吸收﹐绝对生物利用度接近100%﹐约10小时达到稳态浓度。在用平均剂量9.3ng/kg/min治疗的患者中﹐浓度约为2000pg/ml。
分布
中央室中药物的分布体积约为14L/70kg(理想体重)。体外研究显示﹐在330~10000μ g/L的浓度范围内﹐曲前列尼尔与人血浆蛋白的结合率约为91%。
代谢和排泄
曲前列尼尔主要在肝脏由CYP2C8代谢。在健康志愿者进行的一项研究中﹐皮下注射[C]曲前列尼尔﹐在给药后10天内﹐在尿液和粪便中的标记物分别占给药剂量的78.6%﹑13.4%。仅有4%的药物以原形形式从尿中排出。尿液中检测到五种代谢产物﹐范围为10.2%~15.5%﹐约为给药剂量的64.4%﹐其中四种代谢产物均为3-羟辛基侧链的氧化产物﹐另一个代谢产物是葡糖苷酸共轭衍生物(曲前列尼尔葡糖苷酸)。已鉴定的代谢产物不具有活性。
使用二室模型﹐曲前列尼尔的消除(皮下给药后)为双相性﹐终末消除半衰期约为4h。体重为70kg的患者全身清除率约为30L/h。
体外研究结果显示﹐曲前列尼尔不抑制或诱导主要CYP酶。
特殊人群
肝功能不全患者
与健康受试者相比﹐门脉性肺动脉高压和轻度(n=4)或中度(n=5)肝功能不全患者﹐以10ng/kg/min皮下输注本品150分钟﹐C max 分别增加2倍和4倍﹐AUC 0-∞ 分别增加3倍和5倍。与健康成年人相比﹐曲前列尼尔在肝功能不全患者的清除率降低﹐降低幅度可高达80%。
肾功能不全患者
尚未在肾功能不全患者中进行研究﹐所以﹐对该类患者的给药剂量无特殊建议。虽然只有4%的药物以原形形式从尿中排出﹐但已鉴定的五种代谢产物均经尿液排泄。
15~25℃下保存。
欧洲药典/美国药典I型无色玻璃瓶﹐配有溴化丁基胶塞和铝制易拉密封盖:
1)20mg 曲前列尼尔(每1ml 中含 1mg 曲前列尼尔)﹐20ml 玻璃瓶包装﹐1支/盒;
2)50mg 曲前列尼尔(每1ml 中含 2.5mg 曲前列尼尔) ﹐20ml 玻璃瓶包装﹐1支/盒;
3)100mg 曲前列尼尔(每1ml 中含 5mg 曲前列尼尔) ﹐20ml 玻璃瓶包装﹐1支/盒;
4)200mg 曲前列尼尔(每1ml 中含 10mg 曲前列尼尔) ﹐20ml 玻璃瓶包装﹐1支/盒。
36个月
进口药品注册标准JX20120073

详细内容:桐晖药业 -提供原料药、参比制剂、杂质对照品、进口药品注册代理、致力于为客户提供一站式整体解决方案,欢迎来电咨询
中文名称:盐酸特比萘芬乳膏
英文名:Terbinafine Hydrochloride Cream
规格:1%
持证商:GSK Consumer Healthcare Schweiz AG/Karo Healthcare AB
备注1:国内上市的原研药品
备注2:原研进口增加变更后上市许可持有人Karo Healthcare AB
剂型:乳膏剂

产品名称:靛胭脂
英文名:Indigo Carmine
剂型规格:注射液10ml:40mg
适应症:蓝色染料,主要由肾小管排泄。静脉或肌内注10min, 尿液显示蓝色为正常,用于测定肾功能
科室:放射科,影像科
家数:制剂1国
产品优势:1. 国内无原料备案,制剂只有1家2.原料用量少,价值高3.能供此产品的外商也不多
原料来源:印度
备案状态:无


【别名】 靛红;靛卡红;靛蓝二磺酸钠;靛胭脂
【外文名】Indicarmine , Indigo Carmine ,Acid Blue 74
【分子式】C16H8N2Na2O8S2
【分子量】466.35
【适应症】 为蓝色染料,主要由肾小管排泄。用于测定肾功能 .
【用量用法】 静脉或肌内注射后10分钟内尿液如显蓝色为正常。
【规格】 注射液:40mg(10ml)。
正常的消化道粘膜表面是光滑的,而当有微小病变,例如溃疡、癌变等,表面就会发生变化,但是在早期的时候由于变化很小,很难在普通内镜下发现。染色剂利用对比原理,当对粘膜喷洒染色剂后,表面光滑的部分,靛胭脂不能沉积,而全部沉积在粘膜皱襞的沟纹之间,与桔红色粘膜形成鲜明对比,在直视下,形成连续的线条,显示出粘膜的细微凹凸变化及其立体结构,有利于临床上能够在早期发现不明显的肿瘤等病变,为患者及早发现及早治疗提供了条件。利用染色剂沉积后颜色的不同来显现微观结构,属于物理作用,无化学反应发生,并非利用对组织染色来观察,其本身不与粘膜组织发生作用,该色素沉积于粘膜皱襞,不被吸收,也不和粘液结合,经肠道排出体外。

详细内容:桐晖药业 -提供原料药、参比制剂、杂质对照品、进口药品注册代理、致力于为客户提供一站式整体解决方案,欢迎来电咨询
中文名称:盐酸赛洛唑啉鼻用喷雾剂
英文名:Xylometazoline Hydrochloride Nasal Spray
规格:10mL:10mg,总喷次63次,每喷喷量140mg
持证商:GSK Consumer Healthcare Schweiz AG / Haleon Schweiz AG
备注1:国内上市的原研药品
备注2:原研进口增加变更后上市许可持有人Haleon Schweiz AG
剂型:喷雾剂