
【评价原理】
斑马鱼胚胎视力发育迅速,受精后发育4天的幼鱼就已经依赖视觉线索进行捕食和躲避行为。斑马鱼不仅在角膜、晶状体、脉络膜、视网膜以及血管化和神经支配等结构上和人类的眼睛有明显的相似性,而且还有保守的基因表达、细胞构成和组织结构,因此为研究食品及保健品的眼部毒性提供了一个极好的模型。
我们评价斑马鱼眼毒性有4个指标:1.眼睛大小;2.眼部细胞凋亡;3.眼部血管面积;4.眼部病理切片。
【实验方案】
我们将受测试斑马鱼分成两组,分别是正常对照组和供试品组,供试品组(保健食品通过溶解到养鱼用水中或灌胃的方式摄入到斑马鱼体内)。
服用一段时间眼保护剂后,我们在解剖显微镜下观察眼睛大小;整体做凋亡细胞特异性染色,观察眼部细胞凋亡;通过荧光显微镜观察眼部血管面积,同时制作成病理切片观察眼部的病理结构变化。
【结果展示】

图1. 斑马鱼眼睛表型图
箭头指示区域为眼
可以看到,保健食品组眼睛相较于正常对照组明显减小。
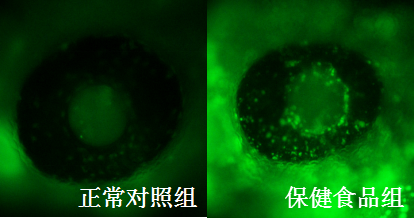
图2. 斑马鱼眼细胞凋亡表型图
黄色虚线区域为眼,绿色小点为凋亡细胞
可以看到,保健食品组的凋亡细胞较正常对照组明显增多。
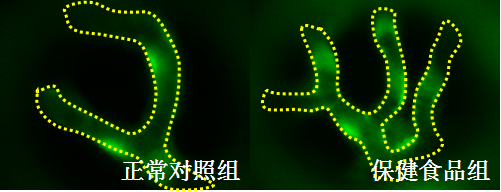
图3. 斑马鱼眼部血管面积
黄色虚线标记血管面积
可以看到,保健食品组眼睛血管面积相较于正常对照组明显增加。
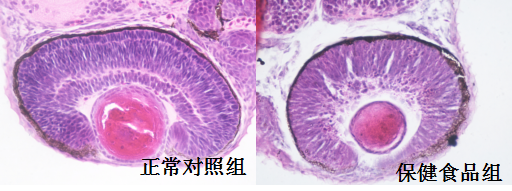
图4. 眼部凋亡细胞病理切片
可以看到,保健食品组出现较多的凋亡细胞,表现为细胞固缩、染色质边集,视网膜结构异于正常对照组。
【评价结论】
1.经过每组30尾斑马鱼的对比实验,保健食品组斑马鱼眼睛明显变小,凋亡细胞明显增多,眼部血管面积明显增多,在病理切片中出现较多的凋亡细胞,表现为细胞固缩、染色质边集,视网膜结构异常。
2.本实验证实了保健食品的眼毒性。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)

【评价原理】
斑马鱼的基因与人类基因的相似度达到87%,斑马鱼肝脏中有许多与哺乳动物同源的脂质代谢酶,与哺乳动物对外源化学物质的防御机制相当,包括酶的诱导和氧化应激。而且斑马鱼幼鱼通体透明,容易观察到毒性表型。
我们评价斑马鱼肝脏毒性有4个指标:1.肝脏面积;2.肝脏变性程度;3. 卵黄囊吸收延迟的发生率(卵黄囊是脂肪,卵黄囊吸收与肝功能密切相关);4. 肝脏病理切片。
【实验方案】
我们将受测试斑马鱼分成两组,分别是正常对照和服用/注射供试品组(供试品通过溶解到养鱼用水中或注射的方式摄入到斑马鱼体内)。
服用/注射药物一段时间后,我们观察斑马鱼肝脏及卵黄囊表型,同时制作成病理切片观察肝脏的病理结构变化。
【结果展示】

图1. 斑马鱼肝脏毒性表型图
可以看到,服用/注射供试品组斑马鱼肝脏肿大、变性、卵黄囊吸收延迟。

图2. 斑马鱼肝脏病理切片
绿色箭头指向红细胞淤积
从病理切片中可见,正常对照组肝组织结构规则,肝细胞形态完整,细胞质均匀,细胞核呈规则圆形,位于细胞中央;服用/注射供试品组的斑马鱼肝脏红细胞淤积严重,细胞肿胀现象严重,细胞核萎缩变形,位于细胞边缘,局部可见炎性浸润,坏死。
【评价结论】
1.经过每组30尾斑马鱼的对比实验,服用/注射供试品组的斑马鱼肝脏产生明显的毒性表型且组织病理学改变,与正常对照组存在明显的差别。
2.本实验证实了该供试品对斑马鱼有肝脏毒性。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)

【评价原理】
肠道消化是食物在消化道中分解的过程,包括机械性消化(通过消化道肌肉搜索将食物与消化液混合并向消化道远端推送)和化学性消化(通过消化腺分泌的消化酶将大分子分解为小分子物质的过程)。肠道内的消化液包括胰脂肪酶、胰蛋白酶、胰淀粉酶等。在受精后的26-126 h,斑马鱼肠道的管腔形成,内胚层分化出连续的有功能的肠道上皮。斑马鱼肠道肌肉发达,可分为两层平滑肌,有利于食物的蠕动消化。
通过特异性的检测试剂盒检测OD值,可以量化斑马鱼体内胰脂肪酶和胰蛋白酶含量。
【实验方案】
我们将受测试斑马鱼分成二组,分别是正常对照和服用供试品组(供试品通过溶解到养鱼用水中或注射的方式摄入到斑马鱼体内),加入相应的胰脂肪酶和胰蛋白酶特异性检测试剂。
服用供试品后,我们使用酶标仪对斑马鱼进行OD值的检测。
【结果展示】
图1. 斑马鱼胰脂肪酶和胰蛋白酶OD值
可以看到,服用供试品组的胰脂肪酶和胰蛋白酶的OD值与正常对照组比较,有显著性提高。
【评价结论】
1.经过每组30尾斑马鱼的对比实验,服用供试品组与正常对照组比较胰脂肪酶和胰蛋白酶含量均有明显的升高。
2.本实验证实了供试品具有促进肠道消化功能的作用,主要表现为增加胰脂肪酶和胰蛋白酶的含量。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)

【评价原理】
肠道消化是食物在消化道中分解的过程,包括机械性消化(通过消化道肌肉搜索将食物与消化液混合并向消化道远端推送)和化学性消化(通过消化腺分泌的消化酶将大分子分解为小分子物质的过程)。肠道内的消化液包括胰脂肪酶、胰蛋白酶、胰淀粉酶等。在受精后的26-126 h,斑马鱼肠道的管腔形成,内胚层分化出连续的有功能的肠道上皮。斑马鱼肠道肌肉发达,可分为两层平滑肌,有利于食物的蠕动消化。
通过特异性的检测试剂盒检测OD值,可以量化斑马鱼体内胰脂肪酶和胰蛋白酶含量。
【实验方案】
我们将受测试斑马鱼分成二组,分别是正常对照和服用供试品组(供试品通过溶解到养鱼用水中或注射的方式摄入到斑马鱼体内),加入相应的胰脂肪酶和胰蛋白酶特异性检测试剂。
服用供试品后,我们使用酶标仪对斑马鱼进行OD值的检测。
【结果展示】

图1. 斑马鱼胰脂肪酶和胰蛋白酶OD值
可以看到,服用供试品组的胰脂肪酶和胰蛋白酶的OD值与正常对照组比较,有显著性提高。
【评价结论】
1.经过每组30尾斑马鱼的对比实验,服用供试品组与正常对照组比较胰脂肪酶和胰蛋白酶含量均有明显的升高。
2.本实验证实了供试品具有促进肠道消化功能的作用,主要表现为增加胰脂肪酶和胰蛋白酶的含量。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)

【评价原理】
便秘的主要表现是排便次数减少和排便困难。斑马鱼是一种与人类同源性较高的脊椎动物,它的肠道组成与人类相似,具有内皮细胞、结缔组织、环状肌肉和外纵肌层。硫酸铝能减少肠道蠕动,诱发斑马鱼便秘。
经过喂食不被肠道吸收的特异性荧光材料,可以明显的观察到被便秘斑马鱼肠道蠕动减慢,肠道内的荧光强度明显比正常斑马鱼亮。
【实验方案】
我们将受测试斑马鱼分成三组,分别是正常对照组、模型对照组和服用通便剂组。服用通便剂组提前服用一段时间吗丁啉、派立清口服液和慈素粉之类的通便剂后,正常对照组、模型对照组与服用通便剂组都摄入了等量荧光材料。荧光材料摄入后,正常对照组不做任何处理,模型对照组和服用通便剂组都摄入了等量硫酸铝(荧光材料和硫酸铝通过溶解到养鱼用水中的方式摄入到斑马鱼体内)。
服用一段时间通便剂后,我们在荧光显微镜下观察斑马鱼肠道荧光强度。
【结果展示】

图1. 斑马鱼肠道荧光强度表型图
可以看到,服用通便剂组的肠道荧光强度较模型对照组明显减弱。
【评价结论】
1.经过每组30尾斑马鱼的对比实验,服用通便剂组的肠道荧光强度较模型对照组明显减弱。
2.本实验证实了吗丁啉、派立清口服液和慈素粉等具有明显通便功效。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)

化妆品中刺激性物质作用于机体后可能引发机体产生刺激、过敏等一系列的反应,其中主要的是刺激反应,可导致水肿、红斑、瘙痒、疼痛等症状。
化妆品对皮肤的刺激表型主要表现为皮肤炎症,炎症早期主要表现为毛细血管扩张、通透性亢进和水肿。
【评价原理】
刺激物进入斑马鱼体内,诱导炎症反应,中性粒细胞发生免疫应答,向皮肤表皮迁移并聚集。通过在荧光显微镜下对斑马鱼皮肤表面的中性粒细胞进行计数,从而反映受试物刺激性强度。
【实验方案】
将受测试斑马鱼分成两组,分别是正常对照和化妆品组(供试品通过溶解到标准稀释水中的方式摄入到斑马鱼体内)。
使用化妆品一段时间后,将斑马鱼整体放到荧光显微镜下拍照,以皮肤表面中性粒细胞数量评价化妆品的刺激性。
【结果展示】

图1. 斑马鱼皮肤中性粒细胞表型图
黄色虚线区域为计算区域
可以看到,化妆品组斑马鱼皮肤表面中性粒细胞数量显著上升。
【评价结论】
1、经过各组斑马鱼的对比实验,化妆品组的斑马鱼皮肤表面中性粒细胞数量明显增多,与正常对照组存在明显的差别。
2、本实验证实了该化妆品对斑马鱼有刺激性。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)

【评价原理】
药物骨毒性的安全性研究与肝、肾、心脏毒性等一般毒性相比较为薄弱,尤其是儿科人群用药的骨毒性安全问题,骨毒性非临床安全性评价愈加受到重视。斑马鱼是一种与人类同源性较高的脊椎动物,和哺乳动物一样,斑马鱼的骨骼是从3种胚胎干细胞系即神经嵴、体节中胚层和侧板发育而来的。
斑马鱼骨骼经过特异性的荧光染色后,经荧光显微镜采集到荧光强度能反映出骨密度和脊椎骨的数量,从而评价供试品骨毒性。
【实验方案】
我们将受测试斑马鱼分成两组,分别是正常对照和供试品组(供试品通过溶解到养鱼用水中或注射的方式摄入到斑马鱼体内)。
服用/注射供试品一段时间后,我们对斑马鱼整体做骨钙染色,以脊椎骨荧光强度和脊椎骨数量评价供试品的骨毒性。
【结果展示】

图1. 斑马鱼骨密度表型图
黄色虚线区域为计算用脊椎骨
可以看到,服用/注射供试品组斑马鱼脊椎骨荧光强度明显减弱。

图2. 斑马鱼脊椎骨数量表型图
可以看到,服用/注射供试品组斑马鱼脊椎骨数量明显减少。
【评价结论】
1.经过每组30尾斑马鱼的对比实验,服用/注射供试品组的斑马鱼脊椎骨荧光强度明显减弱、数量明显减少,与正常对照组存在明显的差别。
2.本实验证实了该供试品对斑马鱼有骨毒性。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)
● 项目意义
肿瘤类器官是将肿瘤患者的新鲜组织经体外3D培养系统建立的、与肿瘤患者特征高度相似的一种立体模型,已被证实与患者肿瘤的病理组织学特征、分子特征、药物敏感性等保持高度一致,在对应的药物筛选领域有着巨大的应用空间。
同时,环特生物已建立的多癌种实体瘤斑马鱼PDX药敏评价体系已用于临床,为患者提供精准的用药指导。我们基于真实世界肿瘤患者的临床研究,联合国内知名三甲医院,开展全世界首个胃癌斑马鱼PDX与患者治疗效果的一致性评价项目(美国临床研究Clinical Trials注册号:NCT05616533),为斑马鱼PDX的临床应用提供更加充分的科学依据。
为满足不同科研场景的行业需求,环特生物联合该医院共同发起“基于胃癌的斑马鱼PDX与类器官抗肿瘤药效评价的科研项目”,通过构建胃癌的精准医疗生物样本库,致力于为广大药企的抗肿瘤药物提供药效评价的科研服务。
● 预期成果
1)构建不少于50例基于胃癌的类器官生物样本库,并完成类器官样本的临床信息、基因信息的采集
2)按需交付药物在胃癌斑马鱼PDX或类器官模型中的定性、定量数据
3)共同产出数篇国际前沿的科研论文
4)实现相关课题项目、技术创新奖项的申报
● 合作伙伴权益
标准权益——
1)享有项目所述样本库的“联合建设单位”两年冠名权
2)享有该项目最终成果的宣传权利
3)项目结束后,一定期限内享受特定数量的药物药效评价折扣
定制(付费)权益——
1)类器官药物研发平台建设(含培训1-3名类器官技术人员、胃癌类器官构建方法的技术转让)
2)其他相关需求及服务
● 项目分工
1)合作医院负责提供胃癌肿瘤组织样本
2)环特生物负责斑马鱼PDX与类器官样本库的构建服务与药效评价
3)药合作伙伴负责根据实际科研需求提供药物和科研经费
● 申报条件
1)具有一定新药研发经验的大中型药物研发机构
2)药物类型为胃癌的化疗药物、靶向药物(免疫类药物除外)、中药,以及辅助治疗的相关药物
● 合作伙伴名额
预计招募合作单位3家
● 项目周期
5-6个月
● 合作详询:成先生 17364531293


【评价原理】
蛋黄粉中60%为脂类,用蛋黄粉喂食斑马鱼,可以使斑马鱼血液中的脂肪含量快速升高,从而建立斑马鱼高血脂症模型。
经过油红O特异性脂肪染色(与组织内甘油三酯等脂肪滴结合呈橘红色),高血脂斑马鱼血管内肉眼可见明显的脂质聚积。
【实验方案】
我们先将测试斑马鱼喂食蛋黄粉(蛋黄粉通过溶解到养鱼用水中的方式摄入到斑马鱼体内),建立高血脂模型后,再将受测试斑马鱼分成三组,分别是正常对照组(不喂食蛋黄粉),模型对照组和服用降脂剂组,服用降脂组摄入阿托伐他汀钙之类的降脂剂。
服用一段时间降脂剂后,我们对斑马鱼整体做脂肪特异性染色,观察体内脂质聚积的变化。同时利用甘油三酯试剂盒检测斑马鱼体内甘油三酯含量的变化。
【结果展示】

图1. 斑马鱼血脂表型图
橘红色脂滴为血脂
可以看到,服用降脂剂组的血脂聚积情况与模型对照组比较明显减少。

图2. 斑马鱼甘油三酯含量(mmol/gprot)
与模型对照组比较,*** p < 0.001
从生化指标可以看出,服用降脂剂组的斑马鱼整体甘油三酯含量与模型对照组比较明显降低。
【评价结论】
1.经过每组30尾斑马鱼的对比实验,服用降脂产品组的血脂聚积情况和整体甘油三酯含量与模型对照组比较明显减少。
2.本实验证实了降脂产品具有显著的降脂作用。
更多项目服务,请拨电话咨询:0571-83782130,项目经理手机 17364531293(微信同号)