该商家已通过实名认证
该商家已通过实名认证
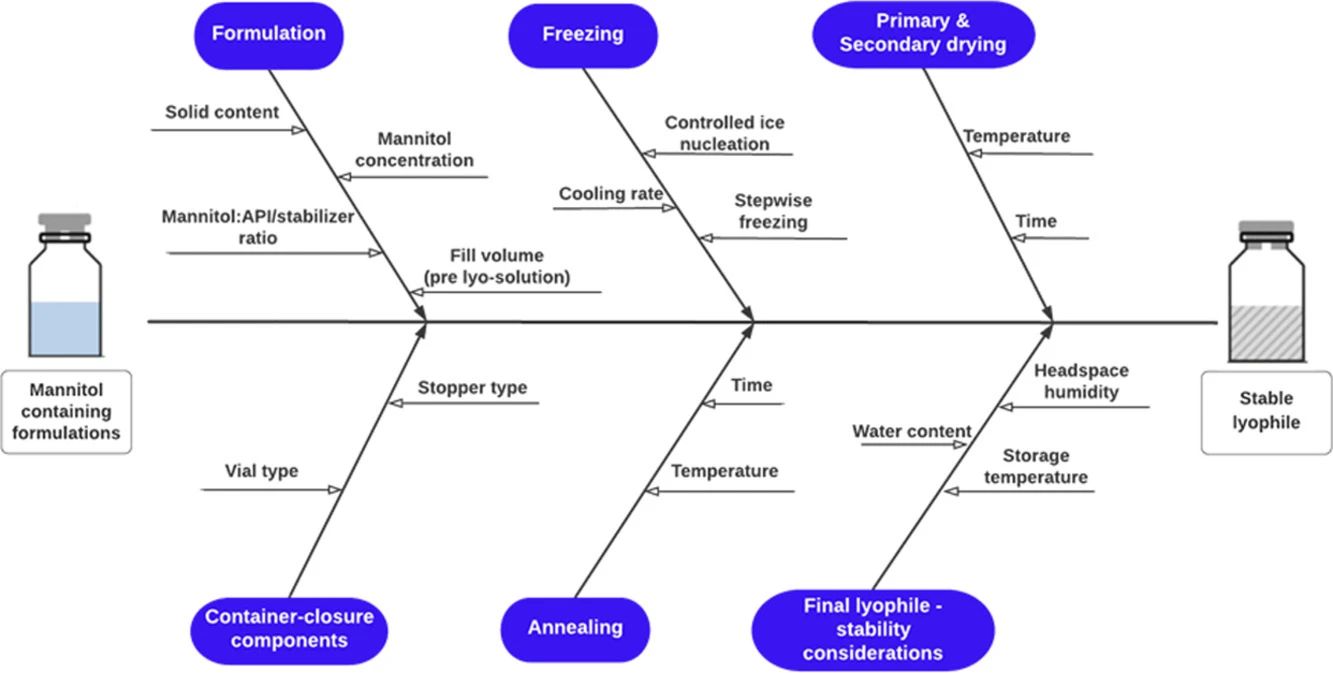
冷冻干燥简称冻干是将需要干燥的药物溶液预先冻结成固体然后在低温低压条件下从冻结状态不经过液 态而直接升华除去水分的一种干燥方法由于整个操作过程都处于低温状态故这种方法尤其适用于热敏性蛋白质药物制剂的制备。而冻干后的蛋白质药物呈疏松状饼块样,不仅有利于保存而且有利于蛋白质药物重溶后的复性。显然,冻干技术为理化性质不稳定的蛋白质药物制剂提供了一种有效的制备方法然而冻干过程是一个复杂的相变过程,在冻结、冻融、干燥和储存过程中存在着多种诱导药品中蛋白质变性的因素,故常需使用一些保护剂来稳定处方中的蛋白质。
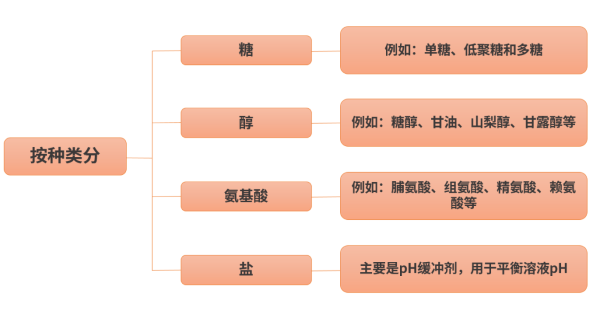
糖类,冻干品中最常用的赋形剂,其结构中的羟基,可以取代蛋白质和水之间的的氢键来提供稳定的效果,是蛋白质的非特异性稳定剂,在冻干的各个阶段(如冷冻、冻融及升华干燥等)均能对蛋白质药物起到一定的保护作用。糖的保护作用与其及蛋白质的种类有关,而双糖是研究最多也公认最有效的保护剂,其中蔗糖是由一分子葡萄糖及一分子果糖所构成的双糖,化学性质稳定,多呈无定型结构,对阻止蛋白质二级结构改变、冻干处理过程中及贮藏期内蛋白质的伸展和聚集起显著作用。与蔗糖相比,海藻糖具有更高的玻璃化温度、更低的引湿性、更不具有还原性,这些优点均预示着海藻糖可能具有更广阔的应用前景。
醇类,像甘露醇一般用作填充剂,其在慢速冻结时会结晶,从而为活性组分提供支撑结构,且不与活性组分发生反应。
D-Mannose
( 甘露糖 )
甘露糖,是一种单糖,溶于水,微溶于乙醇。无色或白色结晶粉末。在人体代谢过程中,尤其在特定蛋白的糖基化过程中起到重要作用。甘露糖很难被人体所吸收,摄入人体之后很快就会被人体排出体外,主要是经过肾脏代谢,代谢整体周期大概在八个小时左右。摄入甘露糖并不会引起血糖升高,所以对于一些糖尿病患者来说是可以食用的一种糖。
在自然界中,甘露糖以游离状态存在于一些水果中,比如蔓越莓,苹果、橘子等。在人体中,甘露糖则分布在各个组织和血液中,包括皮肤、脏器和神经中。在这些组织中,甘露糖会参与糖蛋白的合成,调节自身免疫系统功能。以往有临床研究表明,甘露糖能够治疗和预防尿路感染,所以国外有一些以甘露糖为主要成分的保健品被用来维护泌尿系统健康。
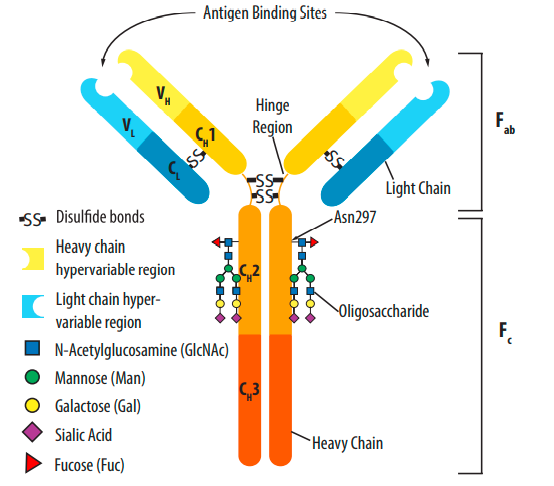
*单克隆抗体结构
单克隆抗体是蛋白类大分子,具有复杂的结构特征,主要由Fab和Fc两大功能区组成,在Fab和Fc段特定的位点存在糖基化修饰。糖基化修饰在维持抗体分子的空间构象、稳定抗体的结构、维持抗体的生物学功能等方面发挥着重要的作用,进而对药物半衰期、有效性和安全性产生影响,故糖基化通常是抗体类药物的CQA(Critical Quality Attributes)之一,各国药品监管机构均要求对抗体类药物的糖基化程度进行严格的控制。
单抗Fc段通常有2个保守的N-糖基化位点(Asn 297,如图所示),N-糖修饰通常在内质网和高尔基体内加工完成,起初由2个N-乙酰葡萄糖胺(N-acetylglucosamine,GlcNAc)、九个甘露糖(Mannose,Man)以及三个葡萄糖(Glucose,Glc)分子通过焦磷酸键与多萜醇结合成糖链分子,运送至Asn并与之相互连接,而后通过一些列酶切作用切除3个葡萄糖和6个甘露糖,形成糖链核心结构,随后在相关糖基转移酶的作用下逐步连上岩藻糖、半乳糖、唾液酸等其他单糖,在糖链形成的过程中,由于甘露糖酶切不完全而形成的5~9个高甘露寡糖(Man9-Man5)被称为高甘露糖糖型。
提升的高甘露糖型含量将会提高抗体药效(主要增强ADCC效应),但会降低药物半衰期(加快体内清除速率)并且具有较强的免疫原性。在新抗体药物研发的早期,一般将甘露糖型Man5的含量控制在10%以下认为是可接受的范围(通常为5%),高甘露糖的形成受到细胞株、培养参数等多因素的影响,本文旨在总结单抗药物高甘露糖修饰的五种调控方法,为控制高甘露糖修饰含量提供参考。
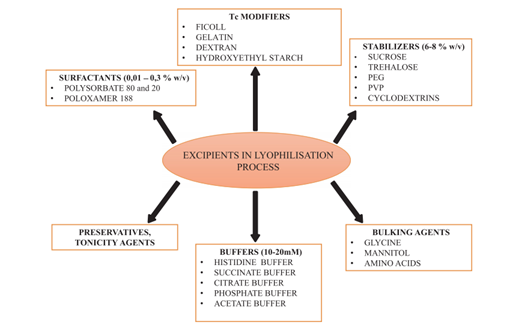
*生物制品冻干制剂常用药用辅料选用
D-Mannitol
( 甘露醇 )
甘露醇是一种糖醇,通常由糖(甘露糖)还原而来,是山梨糖醇的同分异构体,易溶于水,为白色结晶性粉末,有类似蔗糖的甜味。甘露醇不仅可作为优良的骨架剂使用,而且在一些处方中它能够兼作蛋白质的冻干保护剂。甘露醇对蛋白质的保护作用与其浓度、形态结构有关,而其浓度与结晶形态有时呈一定的关联性。通常认为无定型甘露醇具有使蛋白质稳定的作用而结晶态的甘露醇则失去保护功能;1%或更低浓度的甘露醇通过无定型结构的形成而阻止蛋白质药物的聚集,但是高浓度的甘露醇则易于形成结晶态而促进蛋白质药物的聚集。
对于大多数蛋白,重悬后在4℃仅能短期保存(约1周)。如想长期保存,建议先配制成稀释液(其中必须含有载体蛋白,如0.1% BSA,5%HSA,或10% FBS),然后分装冻存于-20℃或-80℃。一定要避免反复冻融,因每次冻融均会引起蛋白的部分失活。
通常加8%(质量比体积)的海藻糖和甘露醇作为冻干保护剂。海藻糖可明显阻止蛋白质二级结构改变以及冻干过程中蛋白质的伸展和聚集;甘露醇也是一种普遍应用的冻干保护剂和填充剂,可以降低某些蛋白的冻干后聚集情况。
填充剂能为冻干饼提供适当的结构,有助于冻干饼块的适当形态,形成孔结构,孔隙率是冷冻水升华的先决条件,较大的孔隙可以更快地升华,因此可以减少初级干燥时间。添加填充剂可实现更短的初级干燥(产品温度Tp˃Tg'或Tc)时间,可作为优化生物制药冻干过程的方法。
通常稳定剂与填充剂的比例应至少为1:2,以提供必要的填充剂结晶。形成的晶格为处于无定形状态的成分提供机械支撑。在 Tg'上方,制剂体系形成的无定形状态刚性不够,无法支撑其自身重量,并且会坍缩到晶体网络上。由于机械支撑,尽管干燥温度高于Tg'(甚至高于Tc),但仍可以防止塌陷发生。在蛋白质浓度<50 mg/mL的处方中,添加填充剂尤为重要,因为在蛋白质浓度较高的配方中体系的Tg′会增加。但如果填充剂在冻干过程中保持无定形状态,由于储存过程中潜在的结晶,可能会影响蛋白质稳定性,因此,通常加入退火步骤可促进填充剂的结晶。