 该商家已通过实名认证
该商家已通过实名认证西安天正药用辅料有限公司,位于古都西安,进驻国亨化工市场。致力于药用辅料行业,秉承为客户提供优质服务,供应优质合格产品为己任,期待您的光临合作。 公司主要经营范围:公司主要给医院制剂室、皮肤所、防疫站、学校、卫生院、实验室、保健品厂、药厂等需要药用辅料的单位,提供各种医药辅料,试剂,中间体,提取物,消毒产品,化工原料和精细化学品等。此外为了满足客户需要我公司推出送货服务(凡是西安市二环内,购买2件产品,我公司给予免费送货服务。)
[更多详情]
[14807-96-6] 本品系滑石经精选、净制、粉碎、干燥制成。主要成分为Mg3Si4O10(OH)2。本品含镁(Mg)应为17.0%~19.5%。 【性状】本品为白色或类白色、无砂性的微细粉末。 本品在水、稀盐酸或8.5%氢氧化钠溶液中均不溶。 【鉴别】(1)取本品0.2g,置铂坩埚中,加等量氟化钙或氟化钠粉末,搅拌,加硫酸5ml,微热,立即将悬有1滴水的铂坩埚盖盖上,稍等片刻,取下铂坩埚盖,水滴出现白色浑浊。 (2)取本品0.5g,置烧杯中,加入盐酸溶液(4→10)10ml,盖上表面皿,加热至微沸,不时摇动烧杯,并保持微沸40分钟,取下,用快速滤纸滤过,用水洗涤滤渣4~5次。取滤渣约0.1g,置铂坩埚中,加入硫酸溶液(1→2)10滴和氢氟酸5ml,加热至冒二氧化硫白烟时,取下,冷却,加水10ml使溶解,取溶液2滴,加镁试剂(取对硝基苯偶氮间苯二酚0.01g,加4%氢氧化钠溶液1000ml溶解,即得)1滴,滴加40%氢氧化钠溶液使成碱性,生成天蓝色沉淀。 (3)本品的红外光吸收图谱应在3677cm-1±2cm-1,1018cm-1±2cm-1,669cm-1±2cm-1波数处有特征吸收(通则0402)。 【检查】酸碱度 取本品10.0g,加水50ml,煮沸30分钟,时时补充蒸失的水分,滤过,滤液遇石蕊试纸应显中性反应。 水中可溶物 取本品10g,精密称定,置250ml具塞锥形瓶中,精密加水50ml,称重,摇匀,加热回流30分钟,放冷,再称重,用水补足减失的重量,摇匀,必要时离心,取上清液,用0.45μm孔径的滤膜滤过,精密量取续滤液25ml,置恒重的蒸发皿中蒸干,在105℃干燥1小时,遗留残渣不得过5mg(0.1%)。 酸中可溶物 取本品1g,精密称定,置100ml具塞锥形瓶中,精密加入稀盐酸20ml,称重,摇匀,在50℃静置15分钟,放冷,再称重,用稀盐酸补足减失的重量,摇匀,必要时离心,取上清液,用0.45μm孔径的滤膜滤过,精密量取续滤液10ml,置恒重的坩埚中,加稀硫酸1ml,蒸干,低温加热至硫酸蒸气除尽后,在700~800℃炽灼至恒重,遗留残渣不得过10mg(2.0%)。 石棉 取本品,置载样架中,压实,照X射线衍射法(通则0451第二法)测定,以Cu为阳极靶,Kα线为特征X射线,管电压为40kV,管电流为40mA,采用连续扫描方式,分别在衍射角(2θ)10°~13°与24°~26°的范围内,以每分钟0.02°的速度扫描,记录衍射图谱。若供试品在衍射角(2θ)10.5°±0.1°处出现角闪石的特征峰,或在衍射角(2θ)12.1°±0.1°与24.31°±0.1°处出现蛇纹石特征峰[1],将供试品置光学显微镜下观察(通则2001),不得出现长宽比大于20或长度超过5μm的细针状纤维;或不得岀现以下情况中的2项及以上:①成束状的平行纤维;②纤维束末端呈发散性;③薄针状纤维;④由单个纤维缠绕而成的团块或弯曲状纤维。 炽灼失重 取本品约2g,精密称定,在600~700℃炽灼至恒重,减失重量不得过5.0%。 铁 取本品约10g,精密称定,置锥形瓶中,加0.5mol/L盐酸溶液50ml,摇匀,水浴加热回流30分钟,放冷,用中速滤纸滤过,滤液置100ml量瓶中,用热水30ml分次洗涤容器及滤渣,滤过,洗液并入同一量瓶中,放冷,加水至刻度,摇匀,作为供试品贮备液,精密量取5ml,置200ml量瓶中,用0.25mol/L盐酸溶液稀释至刻度,摇匀,作为供试品溶液;同法制备空白溶液;另精密量取铁标准溶液适量,用0.25mol/L盐酸溶液稀释制成每1ml中含铁5~10μg的系列对照品溶液。取空白溶液、供试品溶液和对照品溶液,照原子吸收分光光度法(通则0406第一法),在248.3nm的波长处测定,计算,即得。含铁不得过0.25%。 铅 取铁盐项下的供试品贮备液作为供试品溶液;除去供试品,同法制备空白溶液;另精密量取铅标准溶液适量,用0.25mol/L盐酸溶液稀释制成每1ml中含铅0.5~1.25μg的系列对照品溶液。取空白溶液、供试品溶液和对照品溶液,照原子吸收分光光度法(通则0406第一法),在217.0nm的波长处测定,计算,即得。含铅不得过0.001%。 钙 精密量取含量测定项下的供试品贮备液5ml,置20ml量瓶中,用混合溶液(取盐酸10ml和8.9%氯化镧溶液10ml,加水至100ml)稀释至刻度,摇匀,作为供试品溶液;同法制备空白溶液;另精密量取钙标准溶液适量,用水稀释制成每1ml中含钙100μg的溶液,精密量取适量,用混合溶液稀释制成每1ml中含钙1~5μg的系列对照品溶液。取空白溶液、供试品溶液和对照品溶液,照原子吸收分光光度法(通则0406第一法),在422.7nm的波长处测定,计算,即得。含钙不得过0.9%。 铝 精密量取含量测定项下的供试品贮备液0.1ml,置100ml量瓶中,加硝酸溶液(2→100)稀释至刻度,摇匀,作为供试品溶液。另精密量取铝标准溶液适量,用硝酸溶液(2→100)定量稀释制成每1ml中含铝40ng的溶液作为对照品溶液。分别取供试品溶液和对照品溶液,以石墨炉为原子化器,必要时,使用0.25%的氯化铯溶液作为基体改进剂,照原子吸收分光光度法(通则0406),在309.3nm的波长处分别测定,供试品溶液的吸光度不得大于对照品溶液的吸光度(2.0%)。 砷盐 取铁盐项下供试品贮备液10ml,加盐酸5ml与水13ml,依法检查(通则0822第一法),应符合规定(0.0002%)。 【含量测定】取本品约0.1g,精密称定,置聚四氟乙烯容器中,加盐酸1ml、硝酸1ml与高氯酸1ml,摇匀,加氢氟酸7ml,置加热板上缓缓蒸至近干(约0.5ml),用硝酸溶液(2→100)转移至50ml量瓶中,并用水稀释至刻度,摇匀,作为供试品贮备液。精密量取贮备液2ml,置50ml量瓶中,用水稀释至刻度,摇匀,精密量取2ml,置100ml量瓶中,用混合溶液(取盐酸10ml和8.9%氯化镧溶液10ml,加水至100ml)稀释至刻度,摇匀,作为供试品溶液。精密量取镁标准溶液适量,分别用水稀释制成每1ml中含镁10μg、15μg、20μg、25μg的溶液,各精密量取2ml,分置100ml量瓶中,用混合溶液稀释至刻度,摇匀,作为对照品溶液。取空白溶液、供试品溶液和对照品溶液,照原子吸收分光光度法(通则0406第一法),在285.2nm的波长处测定,用标准曲线法计算,即得。 微生物限度 取本品,依法检查(通则1105与通则1106),每1g供试品中需氧菌总数不得过103cfu,霉菌和酵母菌总数不得过102cfu,不得检出大肠埃希菌;每10g供试品中不得检出沙门菌。 【类别】药用辅料,润滑剂等。 【贮藏】置干燥处保存。 【标示】应标明粒度的标示值。 注:本品有滑腻感。
滑石粉

联系电话:18892005891
C20H38O2 310.51 本品为脂肪酸乙酯的混合物,主要成分为油酸乙酯。 【性状】本品为无色至淡黄色澄清液体。 本品可与乙醇、二氯甲烷或石油醚(40~60℃)任意混溶,在水中几乎不溶。 相对密度 本品的相对密度(通则0601)为0.866~0.874。 折光率 本品的折光率(通则0622)在25℃时为1.443~1.450。 酸值 本品的酸值(通则0713)应不大于0.5。 碘值 本品的碘值(通则0713)应为75~85。 过氧化值 本品的过氧化值(通则0713)应不大于10.0。 皂化值 本品的皂化值(通则0713)应为177~188。 【鉴别】在脂肪酸组成项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液中油酸乙酯峰的保留时间一致。 【检查】澄清度与颜色 取本品,依法检查(通则0901与通则0902),溶液应澄清无色;如显色,与黄色3号标准比色液(通则0901第一法)比较,不得更深。 水分 取本品,照水分测定法(通则0832第一法1)测定,含水分不得过1.0%。 炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。 脂肪酸组成 取本品适量,精密称定,加正己烷溶解并定量稀释制成每1ml中约含5mg的溶液,作为供试品溶液;另取油酸乙酯、棕榈酸乙酯、亚油酸乙酯与硬脂酸乙酯对照品各适量,加正己烷溶解并稀释制成每1ml中分别约含5mg、1.2mg、1.2mg与0.5mg的混合溶液,作为对照品溶液。照气相色谱法(通则0521)试验,以聚乙二醇(或极性相近)为固定液的毛细管柱为色谱柱,起始温度为178℃,维持2分钟,以每分钟3.3℃的速率升温至240℃,维持2.5分钟;进样口温度为250℃;检测器温度为270℃。取对照品溶液1μl注入气相色谱仪,记录色谱图,硬脂酸乙酯峰与油酸乙酯峰的分离度应不小于2.0。取供试品溶液1μl注入气相色谱仪,记录色谱图。按面积归一化法计算(溶剂峰与峰面积小于0.05%的色谱峰忽略不计),含棕榈酸乙酯不得过16.0%,硬脂酸乙酯不得过6.0%,油酸乙酯不得少于65.0%,亚油酸乙酯不得过18.0%。 【类别】药用辅料,增塑剂和软膏基质等。 【贮藏】遮光,密闭保存。

(C6H10O5)7 1134.99 [7585-39-9] 本品为环状糊精葡萄糖基转移酶作用于淀粉而生成的7个葡萄糖以α-1,4-糖苷键结合的环状低聚糖。按干燥品计算,含(C6H10O5)7应为98.0%~102.0%。 【性状】本品为白色结晶或结晶性粉末。 本品在水中略溶,在甲醇、乙醇或丙酮中几乎不溶。 比旋度取 本品,精密称定,加水使溶解并定量稀释制成每1ml中约含10mg的溶液,依法测定(通则0621),比旋度为+160°至+164°。 【鉴别】(1)取本品约0.2g,加碘试液2ml,在水浴中加热使溶解,放冷,产生黄褐色沉淀。 (2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。 (3)本品的红外光吸收图谱应与对照品的图谱一致(通则0402)。 【检查】酸碱度 取本品约0.20g,加水20ml使溶解,加饱和氯化钾溶液0.2ml,依法测定(通则0631),pH值应为5.0~8.0。 溶液的澄清度与颜色 取本品0.50g,加水50ml使溶解,依法检查(通则0901与通则0902),溶液应澄清无色;如显浑浊,与2号浊度标准液(通则0902第一法)比较,不得更浓。 杂质吸光度 取本品约1g,精密称定,加水100ml使溶解,照紫外-可见分光光度法(通则0401)测定,在230~350nm波长范围内的吸光度不得过0.10,在350~750nm波长范围内的吸光度不得过0.05。 氯化物 取本品0.39g,依法检查(通则0801),与标准氯化钠溶液7.0ml制成的对照溶液比较,不得更浓(0.018%)。 还原糖 取本品约2.0g,精密称定,加水25ml使溶解,加碱性酒石酸铜试液40ml,缓缓煮沸3分钟,室温放置过夜,用4号垂熔漏斗滤过,沉淀用温水洗至洗液呈中性,弃去滤液和洗液,沉淀加热硫酸铁试液20ml使溶解,滤过,滤器用水100ml洗涤,合并滤液与洗液,加热至60℃,趁热用高锰酸钾滴定液(0.02mol/L)滴定。按干燥品计算,每2g消耗高锰酸钾滴定液(0.02mol/L)不得过3.2ml(0.5%)。 残留溶剂 环己烷、三氯乙烯和甲苯 取本品约0.2g,精密称定,置顶空瓶中,加内标溶液(取二氯乙烯适量,用20%二甲基亚砜溶液定量制成每1ml中约含10μg的溶液,即得)10.0ml,作为供试品溶液;另精密称取环己烷、三氯乙烯和甲苯适量,加内标溶液溶解并定量稀释成每1ml中分别含环己烷78μg、三氯乙烯0.2μg、甲苯0.2μg的混合溶液,量取10.0ml置顶空瓶中作为对照品溶液。照残留溶剂测定法(通则0861第二法)试验,以100%二甲基聚硅氧烷为固定液的毛细管柱为色谱柱;柱温为50℃,维持8分钟,以每分钟8℃的速率升温至120℃,维持10分钟;进样口温度为140℃;检测器温度为280℃;顶空瓶平衡温度为70℃平衡时间为30分钟。取对照品溶液顶空进样,各成分峰的分离度应符合要求。取供试品溶液与对照品溶液分别顶空进样,记录色谱图,按内标法以峰面积计算,含环己烷不得过0.388%,三氯乙烯不得过0.001%,甲苯不得过0.001%。 有关物质 取本品适量,精密称定,用水溶解并定量稀释制成每1ml中约含10mg的溶液,作为供试品溶液;精密量取含量测定项下的系统适用性溶液5ml,置50ml量瓶中,用水稀释至刻度,摇匀,作为对照品溶液。照含量测定项下的色谱条件,精密量取供试品溶液和对照品溶液各20μl,分别注入液相色谱仪,记录色谱图至倍他环糊精峰保留时间的2倍。供试品溶液色谱图中如有与阿尔法环糊精、伽马环糊精保留时间一致的色谱峰,其峰面积均不得大于对照品溶液中相应峰的峰面积的一半(0.25%),各杂质峰的峰面积之和不得大于对照品溶液中倍他环糊精的峰面积(0.5%)。 干燥失重 取本品,在105℃干燥至恒重,减失重量不得过14.0%(通则0831)。 炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。 重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之五。 砷盐 取本品1.0g,在500~600℃炽灼使完全灰化,放冷,加水23ml溶解后,加盐酸5ml,依法检查(通则0822第一法),应符合规定(0.0002%)。 微生物限度 取本品,依法检查(通则1105与通则1106),每1g供试品中需氧菌总数不得过103cfu,霉菌和酵母菌总数不得过102cfu,不得检出大肠埃希菌。 【含量测定】照高效液相色谱法(通则0512)测定。 色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂;以水-甲醇(93∶7)为流动相;以示差折光检测器测定,检测器温度40℃,取阿尔法环糊精对照品、倍他环糊精对照品与伽马环糊精对照品适量,加水溶解并定量稀释制成每1ml含上述对照品各0.5mg的混合溶液,作为系统适用性溶液。取50μl注入液相色谱仪,记录色谱图,伽马环糊精峰和阿尔法环糊精峰的分离度应符合要求;各色谱峰的拖尾因子均应在0.8~2.0之间;各色谱峰理论板数均不低于1500。 测定法 取本品约250mg,精密称定,置25ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取5ml,置50ml量瓶中,用水稀释至刻度,摇匀,精密量取50μl注入液相色谱仪,记录色谱图;另取倍他环糊精对照品约25mg,精密称定,置25ml量瓶中,加水溶解并稀释至刻度,摇匀,同法测定。按外标法以峰面积计算,即得。 【类别】药用辅料,包合剂和稳定剂等。 【贮藏】密闭,在干燥处保存。
倍他环糊精

【性状】本品为黑色粉末;无臭;无砂性。 【鉴别】取本品 0.1g,置耐热玻璃管中,在缓缓通入压缩空气的同时,在放置样品的玻璃管处,用酒精灯加热灼烧(注意不应产生明火),产生的气体通入氢氧化钙试液中,即生成白色沉淀。 【检查】酸碱度 取本品 2.5g,加水 50ml,煮沸 5 分钟,放冷,滤过,滤渣用水洗涤,合并滤液与洗液使成 50ml;滤液应澄清,遇石蕊试纸应显中性反应。 氯化物 取酸碱度项下的滤液 10ml,加水稀释成 200ml,摇匀;分取 20ml,依法检查(通则 0801),与标准氯化钠溶液 5.0ml 制成的对照液比较,不得更浓(0.1%)。 硫酸盐 取酸碱度项下剩余的滤液 20ml,依法检查(通则0802),与标准硫酸钾溶液 5.0ml 制成的对照液比较,不得更浓(0.05%)。 未炭化物 取本品 0.25g,加氢氧化钠试液 10ml,煮沸,滤过;滤液如显色,与对照液(取比色用氯化钴液 0.3ml,比色用重铬酸钾液 0.2ml,水 9.5ml 混合制成)比较,不得更深。 酸中溶解物 取本品 1.0g,加水 20ml 与盐酸 5ml,煮沸 5 分钟,滤过,滤渣用热水 10ml 洗净,合并滤液与洗液,加硫酸1ml,蒸干后,炽灼至恒重,遗留残渣不得过10mg。 干燥失重 取本品,在 120℃ 干燥至恒重,减失重量不得过 10.0%(通则 0831)。 炽灼残渣 取本品约 0.50g,加乙醇 2~3 滴湿润后,依法检查(通则 0841),遗留残渣不得过 3.0%。 铁盐 取本品 1.0g,加 1mol/L 盐酸溶液 25ml,煮沸 5 分钟,放冷,滤过,用热水 30ml 分次洗涤残渣,合并滤液与洗液,加水适量使成 100ml,摇匀;精密量取 5ml,置 50ml 纳氏比色管中,依法检查(通则 0807),与标准铁溶液 2.5ml 制成的对照液比较,不得更深(0.05%)。 锌盐 取本品 1.0g,加水 25ml,煮沸 5 分钟,放冷,滤过,用热水 30ml 分次洗涤残渣,合并滤液与洗液,加水适量使成 100ml,摇匀;精密量取 10ml,置 50ml 纳氏比色管中,加维生素C 0.5g,加盐酸溶液(1→2)4ml 与亚铁氰化钾试液 3ml,加水稀释至刻度,摇匀,如发生浑浊,与标准锌溶液[精密称取硫酸锌(ZnSO4·7H2O)44mg,置 100ml 量瓶中,加水溶解并稀释至刻度,摇匀,精密量取 10ml,置另一 100ml 量瓶中,加水稀释至刻度,摇匀,即得。每 1ml 相当于10μg的Zn]2.0ml 用同一方法制成的对照液比较,不得更浓(0.02%)。 重金属 取本品 1.0g,加稀盐酸 10ml 与溴试液 5ml,煮沸 5 分钟,滤过,滤渣用沸水 35ml 洗涤,合并滤液与洗液,加水适量使成 50ml,摇匀;分取 20ml,加酚酞指示液 1 滴,并滴加氨试液至溶液显淡红色,加醋酸盐缓冲液(pH3.5)2ml与水适量使成 25ml,加维生素C 0.5g 溶解后,依法检查(通则 0821 第一法),5 分钟时比色,含重金属不得过百万分之三十。 吸着力 (1)取干燥至恒重的本品 1.0g,加 0.12% 硫酸奎宁溶液 100ml,在室温不低于 20℃ 下,用力振摇 5 分钟,立即用干燥的中速滤纸滤过,分取续滤液 10ml,加盐酸1滴与碘化汞钾试液 5 滴,不得发生浑浊。 (2)精密量取 0.1% 亚甲蓝溶液 50ml 两份,分别置 100ml 具塞量筒中,一支量筒中加干燥至恒重的本品 0.25g,密塞,在室温不低于 20℃ 下,强力振摇 5 分钟,将两支量筒中的溶液分别用干燥的中速滤纸滤过,精密量取续滤液各 25ml,分别置两只 250ml 量瓶中,各加 10% 醋酸钠溶液 50ml,摇匀后,在不断轻微振摇下,各精密加碘滴定液(0.05mol/L)35ml,密塞,摇匀,放置,每隔 10 分钟强力振摇 1 次,50 分钟后,分别用水稀释至刻度,摇匀,放置 10 分钟,分别用干燥滤纸滤过,精密量取续滤液各 100ml,分别用硫代硫酸钠滴定液(0.1mol/L)滴定。两者消耗碘滴定液(0.05mol/L)体积的差值不得少于 1.2ml。 【类别】吸附药。 【贮藏】密封保存。

[9004-65-3] 本品为2-羟丙基醚甲基纤维素,为半合成品,可用两种方法制备:(1)将棉绒或木浆粕纤维用烧碱处理后,再先后与一氯甲烷和环氧丙烷反应,经精制,粉碎得到;(2)用适宜级别的甲基纤维素经氢氧化钠处理,和环氧丙烷在高温高压下反应至理想程度,精制即得。分子量范围为10 000~1 500 000。 根据甲氧基与羟丙氧基含量的不同将羟丙甲纤维素分为四种取代型,即1828、2208、2906、2910型。按干燥品计算,各取代型甲氧基(一OCH3)与羟丙氧基(一OCH2CHOHCH3)的含量应符合下表要求。 【性状】本品为白色或类白色纤维状或颗粒状粉末。 本品在无水乙醇、乙醚或丙酮中几乎不溶;在冷水中溶胀成澄清或微浑浊的胶体溶液。 【鉴别】(1)取本品约1g,加热水(80~90℃)100ml,搅拌形成浆状液体,在冰浴中冷却成黏性液体,取2ml,置试管中,沿管壁缓缓加0.035%蒽酮的硫酸溶液1ml,放置5分钟,在两液接界面处显蓝绿色环。 (2) 取鉴别(1)项下的黏性液体适量,倾注在玻璃板上,俟水分蒸发后,形成一层有韧性的薄膜。 (3) 取本品0.5g,均匀分散于50ml沸水中,用电磁搅拌,形成不溶的浆状物;电磁搅拌下使浆状物冷却至10℃,形成澄清或轻微浑浊的溶液,加水50ml,电磁搅拌并同时加热,以每分钟2~5℃的速度升温,产生浑浊的絮凝温度应不低于50℃。 【检查】黏度 标示黏度小于600mPa・s的,按方法1检验,黏度应为标示黏度的80%~120%;标示黏度大于等于600mPa・s的,按方法2检验,黏度应为标示黏度的75%~140%。 取本品适量(按干燥品计算),加90℃的水制成2.0%(g/g)的溶液,充分搅拌约10分钟,直至颗粒得到完全均匀的分散和润湿且瓶内壁无未溶解的样品颗粒,置冰浴中冷却,冷却过程中继续搅匀,除去气泡,必要时用冷水调节重量,除去所有的泡沫作为供试品溶液。 方法1:在20℃±0.1℃,按流出时间不少于200秒,选用适宜内径的乌氏黏度计测定溶液的运动黏度(ν)(通则0633第一法),并在相同条件下测定溶液的密度(ρ),按下式计算动力黏度(η)=ρν。 方法2:在20℃±0.1℃,选用适宜的单柱型旋转黏度计(Brookfieldtype LV model 或相当的黏度计)按下表条件测定(通则0633第三法),旋转2分钟后读数,停止2分钟,再重复实验2次,取三次实验的平均值。 酸碱度取黏度检查项下的供试品溶液,在20℃士2℃将电极浸泡在供试品溶液中5分钟或至读数稳定后依法测定(通则0631),pH值应为5.0~8.0。 水中不溶物取本品1.0g,置烧杯中,加热水(80~90℃)100ml溶胀约15分钟后,在冰浴中冷却,加水300ml(黏度高的供试品可适当增加水的体积,确保溶液滤过),充分搅拌,用经105℃干燥至恒重的1号垂熔玻璃坩埚滤过,烧杯用水洗净,洗液并入上述垂熔玻璃坩埚中,滤过,在105℃干燥至恒重,遗留残渣不得过5mg(0.5%)。 干燥失重 取本品,在105℃干燥2小时,减失重量不得过5.0%(通则0831)。 炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过1.5%。 重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。 砷盐 取本品1.0g,加氢氧化钙1.0g,混合,加水搅拌均匀,干燥后,先用小火灼烧使炭化,再在600℃炽灼使完全灰化,放冷,加盐酸5ml与水23ml,依法检查(通则0822第一法),应符合规定(0.0002%)。 【含量测定】甲氧基 取本品,照甲氧基、乙氧基与羟丙氧基测定法(通则0712)测定。如采用第一法(气相色谱法),在130℃±2℃条件下加热30分钟后,剧烈振摇5分钟,继续在130℃±2℃条件下加热30分钟,或于130~150℃磁力搅拌或振荡60分钟,其余同法操作。如采用第二法(容量法),取本品,精密称定,依法测定,测得的甲氧基量(%)扣除羟丙氧基量(%)与(31/75×0.93)的乘积,即得。 羟丙氧基 取本品,照甲氧基、乙氧基与羟丙氧基测定法(通则0712)测定。如采用第一法(气相色谱法),在130℃士2℃条件下加热30分钟后,剧烈振摇5分钟,继续在130℃士2℃条件下加热30分钟,或于130~150℃磁力搅拌或振荡60分钟,其余同法操作。如采用第二法(容量法),取本品0.1g,精密称定,依法测定,即得。 【类别】药用辅料,释放阻滞剂、包衣材料等。 【贮藏】密闭保存。 【标示】应标明取代型;用于缓释片剂骨架成形物时,应标明粒度标示值;并以mPa・s为单位标明黏度标示值。
羟丙甲纤维素

联系电话:18892005891
丁基羟基苯甲醚
Dingjiqiangjibenjiami
Butylated Hydroxyanisole
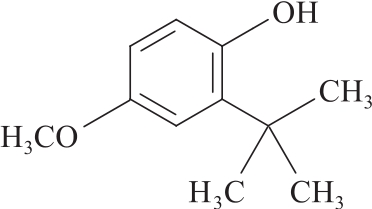
C11H16O2 180.25
[25013-16-5]
本品为2-叔丁基-4-羟基苯甲醚与3-叔丁基-4-羟基苯甲醚的混合物,含C11H16O2不得少于98.5%,其中含2-叔丁基-4-羟基苯甲醚不得过10.0%。
【性状】本品为白色至微黄色或粉红色的结晶性粉末或蜡状固体。
本品在二氯甲烷、乙醇中极易溶解,在水中几乎不溶或不溶。
【鉴别】(1)取本品约0.5mg,加70%乙醇5ml使溶解,加2%硼砂溶液2ml与0.01%氯亚氨基-2,6-二氯醌无水乙醇溶液1ml,摇匀后,溶液显蓝色。
(2)取本品约10mg,加乙醇2ml使溶解,加0.1%丙酸睾酮乙醇溶液1ml与8.5%氢氧化钠溶液2ml, 80℃水浴加热10分钟,放冷,溶液显红色。
(3)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
【检查】有关物质 取本品约50mg,精密称定,置100ml量瓶中,加流动相溶解并稀释至刻度,摇匀,作为供试品溶液。
精密量取供试品溶液1ml,置200ml量瓶中,用流动相稀释至刻度,作为对照溶液。
照含量测定项下的色谱条件试验,精密量取供试品溶液与对照溶液各20μl,分别注入液相色谱仪,记录色谱图至主成分峰保留时间的4倍,供试品溶液的色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.4倍(0.2%),各杂质峰面积的和不得大于对照溶液峰面积(0.5%)。
炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。
重金属 取炽灼残渣项下遗留的残渣,依法检查(通则0821第二法),含重金属不得过百万分之十。
【含量测定】照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验 用十八烷基硅烷键合硅胶为填充剂,以5%冰醋酸溶液(取冰醋酸50ml加水1000ml,混匀)-乙腈(40∶60)为流动相;检测波长为290nm。取2-叔丁基-4-羟基苯甲醚与3-叔丁基-4-羟基苯甲醚对照品适量,加流动相稀释制成每1ml中约含10μg与100μg的混合溶液,取20μl注入液相色谱仪,记录色谱图,2-叔丁基-4-羟基苯甲醚与3-叔丁基-4-羟基苯甲醚的分离度应符合要求。
测定法 取本品约10mg,精密称定,置100ml量瓶中,加流动相溶解并稀释至刻度,摇匀,作为供试品溶液,精密量取20μl注入液相色谱仪,记录色谱图;另取2-叔丁基-4-羟基苯甲醚与3-叔丁基-4-羟基苯甲醚对照品适量,分别用流动相稀释制成每1ml中各含10μg与100μg的溶液,作为对照品溶液,同法测定,按外标法以峰面积分别计算2-叔丁基-4-羟基苯甲醚和3-叔丁基-4-羟基苯甲醚的含量,并计算总和,即得。
【类别】抗氧剂。
【贮藏】遮光,密封,置阴凉处保存。
注:本品具有特异性气味。

联系电话:18892005891
C12H22O11·H2O 360.31 [5989-81-1] 本品为4-O-β-D-吡喃半乳糖基-D-葡萄糖一水合物。按无水物计算,含C12H22O11应为98.0%~102.0%。 【性状】本品为白色至类白色的结晶性颗粒或粉末。 本品在水中易溶,在乙醇、三氯甲烷或乙醚中不溶。 比旋度 取本品10g,精密称定,用80ml的水溶解并加热至50℃,冷却后,加氨试液0.2ml,静置30分钟,用水稀释至100ml,依法测定(通则0621)。按无水物计算,比旋度应为+54.4°至+55.9°。 【鉴别】(1)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。 (2)本品的红外光吸收图谱应与对照图谱(光谱集256图)一致(通则0402)。 【检查】酸碱度 取本品6.0g,加新沸放冷的水25ml溶解,加入酚酞指示液0.3ml,溶液应无色,用氢氧化钠滴定液(0.1mol/L)滴定,至溶液显粉红色,消耗的氢氧化钠滴定液(0.1mol/L)应不得过0.4ml。 溶液的澄清度 取本品1.0g,加沸水10ml溶解后,依法检查(通则0902),溶液应澄清,如显浑浊,与1号浊度标准液比较,不得更浓。 有关物质 取本品适量,加水溶解并定量稀释制成每1ml含100mg的溶液,作为供试品溶液;精密量取1ml,置100ml量瓶中,加水稀释至刻度,摇匀,作为对照溶液。照含量测定项下的方法试验,记录色谱图至主成分峰保留时间的2倍。供试品溶液的色谱图中除溶剂峰以外,如显杂质峰,各杂质峰面积之和不得大于对照溶液主峰面积的0.5倍(0.5%)。 蛋白质与杂质吸光度 取本品,精密称定,加温水溶解并定量稀释成每1ml中含100mg的溶液,照紫外-可见分光光度法(通则0401)检测,在400nm的波长处测定吸光度,不得过0.04。再精密吸取上述溶液1ml,置10ml量瓶中,加水稀释至刻度,照紫外-可见分光光度法(通则0401)检测,在210~220nm的波长范围内测定吸光度,不得过0.25;在270~300nm的波长范围内测定吸光度,不得过0.07。 干燥失重 取本品,在80℃干燥2小时,减失重量不得过1.0%(通则0831)。 水分 取本品,以甲醇-甲酰胺(2∶1)为溶剂,照水分测定法(通则0832第一法1)测定,含水分应为4.5%~5.5%。 炽灼残渣 取本品1.0g,依法检查(通则0841),遗留残渣不得过0.1%。 重金属 取本品3.0g,加温水20ml溶解后,再加醋酸盐缓冲液(pH3.5)2ml与水适量使成25ml,依法检查(通则0821第一法),含重金属不得过百万分之五。 砷盐 取炽灼残渣项下残留物,加水23ml溶解后,加盐酸5ml,依法检查(通则0822第一法),应符合规定(0.0002%)。 微生物限度 取本品,依法检查(通则1105与通则1106),每1g供试品中需氧菌总数不得过103cfu,霉菌和酵母菌总数不得过102cfu,不得检出大肠埃希菌。 【含量测定】照高效液相色谱法(通则0512)测定。 色谱条件与系统适用性试验 用氨基键合硅胶(或氨基键合聚合物)为填充剂;以乙腈-水(70∶30)为流动相;示差折光检测器;参考条件(柱温为30℃,检测器温度为30℃)。取乳糖对照品与蔗糖对照品各适量,精密称定,加水溶解并稀释制成每1ml各含5mg的溶液,取10μl,注入液相色谱仪,乳糖峰与蔗糖峰的分离度应符合要求。 测定法 取本品适量,精密称定,加水溶解并定量稀释制成每1ml约含乳糖5mg的溶液,精密量取10μl,注入液相色谱仪,记录色谱图;另取乳糖对照品适量,同法测定,按外标法以峰面积计算,即得。 【类别】药用辅料,填充剂和矫味剂等(供非注射剂、非吸入制剂用)。 【贮藏】密闭保存。

C12H22O11 342.30 [99-20-7] C12H22O11·2H2O 378.33 [6138-23-4] 本品由食用级淀粉酶解而成。为两个吡喃环葡萄糖分子以1,1-糖苷键连接而成的非还原性双糖,可分为无水物和二水合物。按无水物计算,含C12H22O11应为98.0%~102.0%。 【性状】本品为白色或类白色结晶性粉末。 无水海藻糖在水中易溶,在甲醇或乙醇中几乎不溶。二水海藻糖在水中易溶,在甲醇中微溶,在乙醇中几乎不溶。 比旋度 取本品,精密称定,加水溶解并定量稀释制成每 l ml 中约含 100 mg的溶液,依法测定(通则0621),比旋度为+197°至+201°。 【鉴别】(1)取本品 2 g,加水 5 ml 使溶解,取 l ml,加α-萘酚乙醇溶液(1→20)0.4 ml,沿容器壁缓慢加入硫酸0.5ml,溶液即在两液界面处产生紫色环。 (2) 取本品0.2g,加水5ml溶解,作为供试品溶液;取甘氨酸0.2g,加水5ml溶解,作为甘氨酸溶液。量取供试品溶液2ml,加入稀盐酸1ml,室温静置20分钟;再加入氢氧化钠试液4ml和甘氨酸溶液2ml,于水浴中加热10分钟后,溶液不显棕色。 (3) 在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液的主峰保留时间一致。 (4) 本品的红外光吸收图谱应与对照品的图谱一致(通则0402)。 【检查】酸度 取本品1.0g(按无水物计算),加水10ml使溶解,依法测定(通则0631),pH值应为4.5~6.5。 溶液的澄清度与颜色 取本品33.0g(按无水物计算),置100ml量瓶中,加新沸放冷的水充分振摇使溶解,照紫外-可见分光光度法(通则0401),在420nm与720nm波长处测定吸光度。在720nm波长处的吸光度值不得过0.033,420nm与720nm波长处的吸光度差值不得过0.067。 氯化物 取本品0.40g,依法检查(通则0801),与标准氯化钠溶液5.0ml制成的对照液比较,不得更浓(0.0125%)。 硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液2.0ml制成的对照液比较,不得更浓(0.020%)。 可溶性淀粉 取本品l.0g,加水10ml溶解后,加碘试液1滴,不得显蓝色。 有关物质 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含10mg的溶液,作为供试品溶液;精密量取1ml,置100ml量瓶中,用水稀释至刻度,摇匀,作为对照溶液。照含量测定项下的色谱条件,取对照溶液10μl注入液相色谱仪,记录色谱图,主成分峰高的信噪比应大于10;再精密量取供试品溶液和对照溶液各10μl,分别注入液相色谱仪,记录色谱图。供试品溶液色谱图中,除溶剂峰外,供试品溶液主峰之前、之后的杂质峰面积之和分别不得大于对照溶液主峰面积的0.5倍(0.5%)。 水分 取本品,照水分测定法(通则0832)测定,含水分应为9.0%~11.0%;如为无水物,含水分不得过1.0%。 炽灼残渣 取本品,依法检查(通则0841),遗留残渣不得过0.1%。 重金属 取本品4.0g,加水23ml溶解后,加醋酸盐缓冲液(pH3.5)2ml,依法检查(通则0821第一法),含重金属不得过百万分之五。 微生物限度 取本品,依法检查(通则1105与通则1106),每1g供试品中需氧菌总数不得过103cfu,霉菌和酵母菌总数不得过102cfu,不得检出大肠埃希菌;每10g供试品中不得检出沙门菌。 细菌内毒素(供注射用) 取本品,依法检查(通则1143),每1mg海藻糖中含内毒素的量应小于0.05EU。 【含量测定】照高效液相色谱法(通则0512)测定。 色谱条件与系统适用性试验 釆用磺化交联的苯乙烯-二乙烯基苯共聚物为填充剂的强阳离子钠型(或氢型)色谱柱;以水为流动相;流速为每分钟0.4ml;柱温为80℃;示差折光检测器。取麦芽三糖、葡萄糖与海藻糖对照品适量,加水溶解并稀释制成每1ml中各含2.5mg、2.5mg、10mg的溶液,精密量取20μl注入液相色谱仪,重复进样3次,记录色谱图,主峰面积的相对标准偏差不得过2.0%,各色谱峰的分离度应符合要求。 测定法 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含10mg的溶液,作为供试品溶液,精密量取20μl注入液相色谱仪,记录色谱图;另取海藻糖对照品适量,同法测定。按外标法以峰面积计算,即得。 【类别】药用辅料,矫味剂、甜味剂、冷冻干燥辅料、稀释剂、增稠剂和保湿剂等。 【贮藏】密封,阴凉、干燥处保存。

生命之糖” 一 海藻糖,细胞保护剂
众所周知,水是生命的源泉。在各种生物体内,都含有不等量的水。以植物为例,水生植物的含水量可高达98%,而有些沙漠植物的含水量却只有16%。如果低于这个百分比,这些植物细胞中的原生质就会遭受破坏而死去。
可是,有这么一种植物,即便含水量降低到5%以下,几乎成为“干草”,仍然可以保持生命。人们给这类植物取了一个新的名词“隐生生物(Cvrypohidden Life)”。后来科学家们发现,隐生生物其实广泛存在于生物界,这类生物在干燥时脱水,以极低或停滞的新陈代谢形式处在一种保存状态,当环境允许再水化时它们可立即复活。
这类生物在干燥时其组织中的海藻糖(Trehalose)含量都很高。海藻糖可能与隐生现象密切相关:在有水的时候,海藻糖帮助卷柏吸收和储存水分,干燥时,海藻糖可以取代组织中的水,保护细胞免遭脱水的伤害,维持细胞的天然结构,保护生物组织与生命物质不受破坏的作用,从而延续着生命的奇迹!
藻糖对生物体具有神奇的保护作用,在高温、高寒、高渗透压及干燥失水等恶劣环境条件下海藻糖能在细胞表面能形成独特的保护膜,有效地保护蛋白质分子不变性失活,从而维持生命体的生命过程和生物特征。
海藻糖在医药上的应用主要是作为生物分子的特效保护剂和组织细胞的稳定剂。如单抗制剂、血液制品、疫苗、抗体酶、病毒、激素、重组人体蛋白、离体细胞和组织等生物活性物质。与其他种类的保护剂相比,不仅使其可在常温下保存,还可减少因血液污染引起的乙肝和艾滋病的传播,保证生物制品的质量和安全。另外,由于无需冷冻,还可节省巨额的冷链保藏费用。

本品由食用级淀粉酶解而成。为两个吡喃环葡萄糖分子以1,1-糖苷键连接而成的非还原性双糖,可分为无水物和二水合物。按无水物计算,含C12H22O11应为98.0%~102.0%。 【性状】本品为白色或类白色结晶性粉末。 无水海藻糖在水中易溶,在甲醇或乙醇中几乎不溶。二水海藻糖在水中易溶,在甲醇中微溶,在乙醇中几乎不溶。 比旋度 取本品,精密称定,加水溶解并定量稀释制成每 l ml 中约含 100 mg的溶液,依法测定(通则0621),比旋度为+197°至+201°。 【鉴别】(1)取本品 2 g,加水 5 ml 使溶解,取 l ml,加α-萘酚乙醇溶液(1→20)0.4 ml,沿容器壁缓慢加入硫酸0.5ml,溶液即在两液界面处产生紫色环。 (2) 取本品0.2g,加水5ml溶解,作为供试品溶液;取甘氨酸0.2g,加水5ml溶解,作为甘氨酸溶液。量取供试品溶液2ml,加入稀盐酸1ml,室温静置20分钟;再加入氢氧化钠试液4ml和甘氨酸溶液2ml,于水浴中加热10分钟后,溶液不显棕色。 (3) 在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液的主峰保留时间一致。 (4) 本品的红外光吸收图谱应与对照品的图谱一致(通则0402)。 【检查】酸度 取本品1.0g(按无水物计算),加水10ml使溶解,依法测定(通则0631),pH值应为4.5~6.5。 溶液的澄清度与颜色 取本品33.0g(按无水物计算),置100ml量瓶中,加新沸放冷的水充分振摇使溶解,照紫外-可见分光光度法(通则0401),在420nm与720nm波长处测定吸光度。在720nm波长处的吸光度值不得过0.033,420nm与720nm波长处的吸光度差值不得过0.067。 氯化物 取本品0.40g,依法检查(通则0801),与标准氯化钠溶液5.0ml制成的对照液比较,不得更浓(0.0125%)。 硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液2.0ml制成的对照液比较,不得更浓(0.020%)。 可溶性淀粉 取本品l.0g,加水10ml溶解后,加碘试液1滴,不得显蓝色。 有关物质 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含10mg的溶液,作为供试品溶液;精密量取1ml,置100ml量瓶中,用水稀释至刻度,摇匀,作为对照溶液。照含量测定项下的色谱条件,取对照溶液10μl注入液相色谱仪,记录色谱图,主成分峰高的信噪比应大于10;再精密量取供试品溶液和对照溶液各10μl,分别注入液相色谱仪,记录色谱图。供试品溶液色谱图中,除溶剂峰外,供试品溶液主峰之前、之后的杂质峰面积之和分别不得大于对照溶液主峰面积的0.5倍(0.5%)。 水分 取本品,照水分测定法(通则0832)测定,含水分应为9.0%~11.0%;如为无水物,含水分不得过1.0%。 炽灼残渣 取本品,依法检查(通则0841),遗留残渣不得过0.1%。 重金属 取本品4.0g,加水23ml溶解后,加醋酸盐缓冲液(pH3.5)2ml,依法检查(通则0821第一法),含重金属不得过百万分之五。 微生物限度 取本品,依法检查(通则1105与通则1106),每1g供试品中需氧菌总数不得过103cfu,霉菌和酵母菌总数不得过102cfu,不得检出大肠埃希菌;每10g供试品中不得检出沙门菌。 细菌内毒素(供注射用) 取本品,依法检查(通则1143),每1mg海藻糖中含内毒素的量应小于0.05EU。 【含量测定】照高效液相色谱法(通则0512)测定。 色谱条件与系统适用性试验 釆用磺化交联的苯乙烯-二乙烯基苯共聚物为填充剂的强阳离子钠型(或氢型)色谱柱;以水为流动相;流速为每分钟0.4ml;柱温为80℃;示差折光检测器。取麦芽三糖、葡萄糖与海藻糖对照品适量,加水溶解并稀释制成每1ml中各含2.5mg、2.5mg、10mg的溶液,精密量取20μl注入液相色谱仪,重复进样3次,记录色谱图,主峰面积的相对标准偏差不得过2.0%,各色谱峰的分离度应符合要求。 测定法 取本品适量,精密称定,加水溶解并定量稀释制成每1ml中约含10mg的溶液,作为供试品溶液,精密量取20μl注入液相色谱仪,记录色谱图;另取海藻糖对照品适量,同法测定。按外标法以峰面积计算,即得。 【类别】药用辅料,矫味剂、甜味剂、冷冻干燥辅料、稀释剂、增稠剂和保湿剂等。 【贮藏】密封,阴凉、干燥处保存。